题目内容
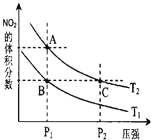
【题目】反应N2O4(g)![]() 2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是
2NO2(g) ΔH=+57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示。下列说法正确的是
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. 由状态B到状态A,可以用加热的方法
D. A、C两点气体的平均相对分子质量:A>C
【答案】C
【解析】试题分析:A、由图像可知,a、c两点都在等温线上,c的压强大,则a、c两点的反应速率:a<c,A错误;B、由图像可知,a、c两点都在等温线上,c的压强大,与a相比c点平衡向逆反应进行,向逆反应进行是由于减小体积增大压强,平衡移动的结果降低NO2浓度增大趋势,但到达平衡仍比原平衡浓度大,平衡时NO2浓度比a的浓度高,NO2为红棕色气体,则a、c两点气体的颜色:a浅,c深,B错误;C、升高温度,化学平衡正向移动,NO2的体积分数增大,由图像可知,a点NO2的体积分数大,则T1<T2,由状态B到状态A,可以用加热的方法,C正确;D、由图像可知,a、c两点都在等温线上,c的压强大,增大压强,化学平衡逆向移动,c点时气体的物质的量小,混合气体的总质量不变,则平均相对分子质量大,即平均相对分子质量:a<c,D错误,答案选C。

练习册系列答案
相关题目