题目内容
15.实验室制取Cl2的反应方程式之一为:2KMnO4+16HCl(浓)═2KCl+2MnCl2+8H2O+5Cl2↑,浓盐酸表现出来的性质是①②(填写编号).①还原性 ②酸性 ③氧化性,被氧化的盐酸占反应盐酸总量的$\frac{5}{8}$;当标准状况下有11.2L氯气生成时,该反应的电子转移数为NA.分析 生成氯气体现浓盐酸的还原性,生成氯化锰体现盐酸的酸性,由Cl原子守恒可知,16molHCl反应时只有10mol作还原剂,该反应中转移10mol电子生成5molCl2,以此来解答.
解答 解:生成氯气体现浓盐酸的还原性,生成氯化锰体现盐酸的酸性,则该反应体现盐酸的性质为①②,由Cl原子守恒可知,16molHCl反应时只有10mol作还原剂,被氧化的盐酸占反应盐酸总量的$\frac{5}{8}$,该反应中转移10mol电子生成5molCl2,当标准状况下有11.2L氯气生成时,该反应的电子转移数为$\frac{11.2L}{22.4L/mol}$×$\frac{10}{5}$×NA=NA,
故答案为:①②;$\frac{5}{8}$;NA.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意盐酸的作用,题目难度不大.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
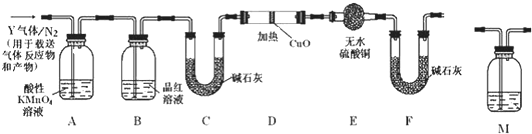
5.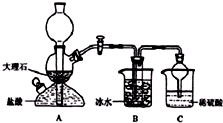 在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
(1)A装置中所发生反应的离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
参照表中数据,请分析B装置中使用冰水是因为温度越低,碳酸氢钠的溶解度越小,便于析出.
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A装置B之间(填写字母)连接一个盛有饱和NaHCO3溶液 的洗气装置,其作用是除去CO2中混有的HCl气体.
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体.请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则
晶体不是NH4HCO3.
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为70%.
 在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
在实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如图实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:(1)A装置中所发生反应的离子方程式为:CaCO3+2H+═Ca2++CO2↑+H2O.C装置中稀硫酸的作用为:吸收从B装置中的试管内逸出的氨气,减少对环境的污染.
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在A装置B之间(填写字母)连接一个盛有饱和NaHCO3溶液 的洗气装置,其作用是除去CO2中混有的HCl气体.
(4)利用改进后的装置进行实验,在B中的试管内析出了晶体,经必要的操作后得到了一种纯净的晶体.请通过简单实验判断该晶体是碳酸氢钠晶体而不是碳酸氢铵晶体,简述操作方法、实验现象及结:取少量晶体置于试管中,在酒精灯上加热使其充分反应后,还有白色固体剩余,则
晶体不是NH4HCO3.
(5)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.88g,则NaHCO3的产率为70%.
6. 在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
回答下列问题:
(1)实验①中,若5min时测得,n(M)=0.050mo1,则0至5min时间内,用N表示的平均反应速率为1.0×10-3mol/(L•min).
(2)实验③平衡常数为1.0,该正反应为放热反应(填“吸热”或“放热”)
(3)能说明上述反应一定达到平衡的条件是C.
A.c(Y)=c(N) B.平均分子量不再变化
C.v正(X)=v逆(M) D.温度和压强一定时,混合气体的密度不再变化
(4)实验③中,达到平衡时,X的转化率为60%多余.
(5)实验③、④中,达到平衡时,a与b的关系为A(填选项),请解释原因若温度不变,则b=$\frac{1}{2}$a,该反应为放热反应,温度升高,平衡向逆反应方向移动,故b<$\frac{1}{2}$a,即a>2b.
A.a>2b B.a=2b C.b<a<2b D.a<b
(6)如图是实验①中c(M)随时间变化的曲线图,请在图中画出实验②中c(M)随时间变化的曲线图.
 在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)所得实验数据如表:| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
(1)实验①中,若5min时测得,n(M)=0.050mo1,则0至5min时间内,用N表示的平均反应速率为1.0×10-3mol/(L•min).
(2)实验③平衡常数为1.0,该正反应为放热反应(填“吸热”或“放热”)
(3)能说明上述反应一定达到平衡的条件是C.
A.c(Y)=c(N) B.平均分子量不再变化
C.v正(X)=v逆(M) D.温度和压强一定时,混合气体的密度不再变化
(4)实验③中,达到平衡时,X的转化率为60%多余.
(5)实验③、④中,达到平衡时,a与b的关系为A(填选项),请解释原因若温度不变,则b=$\frac{1}{2}$a,该反应为放热反应,温度升高,平衡向逆反应方向移动,故b<$\frac{1}{2}$a,即a>2b.
A.a>2b B.a=2b C.b<a<2b D.a<b
(6)如图是实验①中c(M)随时间变化的曲线图,请在图中画出实验②中c(M)随时间变化的曲线图.
3.能证明醋酸是弱酸的事实是( )
| A. | 能溶于水 | |
| B. | 常温下,0.1 mol•Lˉ1醋酸溶液中的c(H+)为1.32×10-3mol•Lˉ1 | |
| C. | 能使紫色石蕊试液变红 | |
| D. | 能被弱碱氨水中和 |
7.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 焰火的五彩缤纷是某些金属元素化学性质的展现 | |
| B. | 将煤气化后再作为能源,可减少PM2.5引起的危害 | |
| C. | 石英用于生产光导纤维和计算机芯片 | |
| D. | 包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同 |
4.下列化学实验操作或事故处理方法正确的是( )
| A. | 如果没有试管夹,可以临时手持试管给固体或液体加热 | |
| B. | 酒精灯不慎碰倒起火时,可用湿抹布或沙子盖灭扑灭,不能用水泼灭 | |
| C. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 | |
| D. | 少量浓硫酸沾到皮肤上时,可立即用大量水冲洗,然后涂上20%~30%的NaOH溶液 |
5.设NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2L氯气含有的分子数为0.5NA | |
| B. | 常温常压下,32gO2和O3的混合气体所含原子数为2NA | |
| C. | 1mol/L CuSO4溶液中含有NA个SO42- | |
| D. | 在电解水实验中,每生成1molH2,就有4NA个电子发生转移 |