题目内容
4.室温下,下列各组离子在指定溶液中能大量共存的是( )| A. | c(H+)=0.1mol/L的溶液:Na+、NH4+、SO42-、S2O32- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液:K+、AlO2-、CO32-、Na+ | |
| C. | 在由水电离出的c(H+)=1×10-12mol/L的溶液:Fe3+、ClO-、Na+、SO42- | |
| D. | c(Fe2+)=0.1mol/L的溶液:H+、Al3+、NO3-、SCN- |
分析 A、在酸性条件下S2O32-发生自身的氧化还原反;
B、$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12<1,溶液呈碱性;
C、由水电离出的c(H+)=1×10-12mol/L的溶液,说明水的电离平衡受抑制,溶液可能是酸性溶液,也可能是碱性溶液;
D、氢离子、硝酸根离子构成强氧化性体系,氧化亚铁离子.
解答 解:A、在酸性条件下S2O32-发生自身的氧化还原反,生成二氧化硫和单质硫,故A错误;
B、$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12<1,溶液呈碱性,该组离子之间不反应,可大量共存,故B正确;
C、由水电离出的c(H+)=1×10-12mol/L的溶液,说明水的电离平衡受抑制,溶液可能是酸性溶液,也可能是碱性溶液,酸性溶液中ClO-不能稳定存在,碱性溶液中,铁离子与氢氧根离子结合生成难溶的氢氧化铁,故C错误;
D、氢离子、硝酸根离子构成强氧化性体系,氧化亚铁离子,所以离子间不能大量共存,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子的反应为解答的关键,侧重分析能力与氧化还原反应、复分解反应的考查,综合性较强,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
2.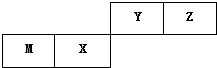 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
 四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )
四种短周期元素在周期表中的位置如图,其中只有M元素原子最外层电子数与电子层数相等,下列说法正确的是( )| A. | 原子半径Z<M | |
| B. | Y的最高价氧化物对应水化物的酸性比X的弱 | |
| C. | 非金属性:X>Z | |
| D. | M元素最高价氧化物对应水化物具有两性 |
3.实验室保存下列试剂,其保存方法和理由描述都正确的是( )
| A. | 固体NaOH,存放在带有橡皮塞的广口瓶中,防止与空气接触被氧化 | |
| B. | 碳酸钠晶体,存放在干燥密封的广口瓶中,防止风化而碎裂成粉末 | |
| C. | 金属钠,存放在有水的广口瓶中,防止氧化 | |
| D. | 过氧化钠粉末,存放在带玻璃塞的细口瓶中,防止吸收水分而变质 |
12.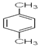 2015年4月在漳州市发生了PX爆炸事件,PX的成分“对二甲苯”,其结构式如图所示:,下列关于PX的叙述中,不正确的是( )
2015年4月在漳州市发生了PX爆炸事件,PX的成分“对二甲苯”,其结构式如图所示:,下列关于PX的叙述中,不正确的是( )
 2015年4月在漳州市发生了PX爆炸事件,PX的成分“对二甲苯”,其结构式如图所示:,下列关于PX的叙述中,不正确的是( )
2015年4月在漳州市发生了PX爆炸事件,PX的成分“对二甲苯”,其结构式如图所示:,下列关于PX的叙述中,不正确的是( )| A. | PX是一种有机化合物 | |
| B. | 仅由碳、氢两种元素组成 | |
| C. | 爆炸燃烧的产物是可能是CO2和H2O | |
| D. | 该有机化合物分子中存在碳碳单键,也存在碳碳双键 |
19.已知去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示.下列说法正确的是( )
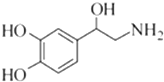

| A. | 去甲肾上腺素的分子式为C8H10O3N | |
| B. | 既能与FeCl3发生显色反应,也能和Na2CO3反应 | |
| C. | 1mol去甲肾上腺素最多能与2mol Br2发生取代反应 | |
| D. | 核磁共振氢谱显示应该有8种不同的氢原子. |
9.氯霉素是一种常见的药物,实验发现由于其分子结构中含有羟基而具有苦味.但如果将其分子中碳链末端的羟基中的氢原子换成来自棕榈酸中的原子团 后,苦味便消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
后,苦味便消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
 后,苦味便消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )
后,苦味便消失,成为便于口服的无味氯霉素.以下关于无味氯霉素的叙述中正确的是( )| A. | 无味氯霉素的水溶性变差,所以苦味消失 | |
| B. | 无味氯霉素失去了药性,所以苦味消失 | |
| C. | 无味氯霉素是棕榈酸的盐类 | |
| D. | 无味氯霉素在人体内不会发生水解 |
16.下列实验能够实现的是( )
| A. | 实验室制取乙烯时用酸性高锰酸钾溶液检验产物 | |
| B. | 除乙酸乙酯中少量的乙酸用足量氢氧化钠溶液充分反应后分液即可 | |
| C. | 检验淀粉水解是否完全将水解液中加碱至碱性后加入碘水 | |
| D. | 苯、硝基苯、乙醇、乙酸四种物质只用碳酸氢钠溶液一种试剂就能鉴别 |
13.下列各组互为同系物的是( )
| A. | CH3( CH2)2 CH3 和 CH3 CH=CH CH3 | |
| B. | CH3( CH2)2 CH3 和 CH3 CH2 CH( CH3) CH2 CH3 | |
| C. | CH3 C≡C CH3 和CH2=CH CH=CH2 | |
| D. | CH3 C≡C CH3 和 CH3 CH=CH CH3 |
14.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,2.24 L CCl4所含的原子数为0.5 NA | |
| B. | 标准状况下0.5mol NO和0.5mol O2组成的混合气体的体积约为22.4L | |
| C. | 78 g Na2O2 与足量水反应转移电子数为NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1 NA |