题目内容
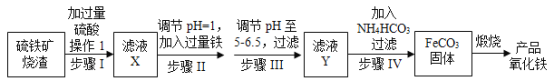
【题目】Ba(NO3)2可用于生产烟花。某主要生产BaCl2、BaCO3、BaSO4的化工厂利用某种钡泥[主要含有BaCO3、Ba(FeO2)2、极少量CuCO3等]制取Ba(NO3)2晶体,其部分工艺流程如下:

已知:Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7。
(1)酸溶时不使用浓硝酸的原因是_________________________________。
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3的反应化学方程式为__________________。
(3)该厂结合本厂实际,中和选用的X为____________(填化学式);中和使溶液中______(填离子符号)的浓度减少(中和引起的溶液体积变化可忽略)。
(4)滤液得到Ba(NO3)2晶体的操作依次为_________、_________、过滤。
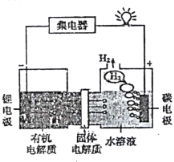
(5)该厂生产的Ba(NO3)2晶体含有少量Cu2+。化学上通过惰性电极电解法富集Cu时,发现电解装置的阴极还有少量使红色石蕊试纸变蓝的气体生成。生成该气体的电极反应为______________________________。
(6)Ba2+致死量为355mg/kg。误食Ba2+可以服用MgSO4溶液解毒,涉及到的离子反应方程式为___________;为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是__________________。
【答案】浓HNO3易挥发、分解 Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O BaCO3 Fe3+、H+ 蒸发浓缩 冷却结晶 NO3-+ 6H2O +8e-=NH3 ↑+ 9OH- Ba2+ + SO42- = BaSO4 ↓ 洗涤废渣并回收洗涤液
【解析】
BaCO3含少量CuCO3、Ba(FeO2)2等杂质,其中Ba(FeO2)2中钡元素为+2价,铁元素为+3价,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有钡离子、铜离子、三价铁离子,可加入X碳酸钡,调节溶液pH=4~5,使铁离子、铜离子水解生成Fe(OH)3沉淀、Cu(OH)2沉淀,过滤后废渣为Fe(OH)3、Cu(OH)2,滤液中主要含有硝酸、硝酸钡,经蒸发浓缩,冷却结晶,过滤可得到硝酸钡晶体,据此分析解答。
BaCO3含少量CuCO3、Ba(FeO2)2等杂质,其中Ba(FeO2)2中钡元素为+2价,铁元素为+3价,加入硝酸,在容器中充分溶解得到溶液,此溶液中含有钡离子、铜离子、三价铁离子,可加入X碳酸钡,调节溶液pH=4~5,使铁离子、铜离子水解生成Fe(OH)3沉淀、Cu(OH)2沉淀,过滤后废渣为Fe(OH)3、Cu(OH)2,滤液中主要含有硝酸、硝酸钡,经蒸发浓缩,冷却结晶,过滤可得到硝酸钡晶体。
(1)酸溶时不使用浓硝酸的原因是浓HNO3易挥发、分解;
(2)酸溶后溶液中pH=1,Ba(FeO2)2与HNO3反应生成硝酸钡、硝酸铁和水,反应的化学方程式为Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;
(3)该厂结合本厂实际,中和选用的X必须能消耗过量硝酸并使铁离子沉淀而除去,且不引入新的杂质,可为BaCO3;中和使溶液中Fe3+、H+的浓度减少;
(4)滤液得到Ba(NO3)2晶体的操作依次为蒸发浓缩、冷却结晶、过滤;
(5)电解装置的阴极还有少量使红色石蕊试纸变蓝的气体生成,则气体显碱性为氨气,生成该气体的电极反应是硝酸根离子得电子产生氨气,电极反应式为NO3-+ 6H2O +8e-=NH3 ↑+ 9OH-;
(6)误食Ba2+可以服用MgSO4溶液解毒,钡离子与硫酸根离子反应产生难溶于酸的硫酸钡,涉及到的离子反应方程式为Ba2+ + SO42- = BaSO4 ↓;为了减少环境污染,请对上述流程中不合理的设计进行改进,改进措施是洗涤废渣并回收洗涤液,避免引起污染。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案