题目内容
【题目】加热熔化氢氧化钠的坩埚,应选用的是( )
A.瓷坩埚B.石英坩埚C.铁坩埚D.铝坩埚
【答案】C
【解析】
A.瓷坩埚主要成分含有SiO2,会与NaOH发生反应,因此不能加热熔化NaOH,错误;
B. 石英坩埚主要成分是SiO2,会与NaOH发生反应,因此不能加热熔化NaOH,错误;
C.铁坩埚在高温下不能与NaOH发生反应,因此可以加热熔化氢氧化钠,正确;
D.铝坩埚的成分Al可以与氢氧化钠发生反应,因此不能加热熔化氢氧化钠,错误。

 阅读快车系列答案
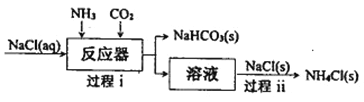
阅读快车系列答案【题目】下列三组实验进行一段时间后,溶液中均有白色沉淀生成,下列结论不正确的是
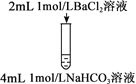
实验① | 实验② | 实验③ |
|
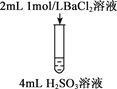
|
|
A. 实验①中生成的沉淀是BaCO3
B. 实验①中有气体生成
C. 实验②沉淀中可能含有BaSO4
D. 实验③生成沉淀的离子方程式是:Ba2++ H2SO3===BaSO3↓+2H+
【题目】为探究 H2O2、SO2、Br2 氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)
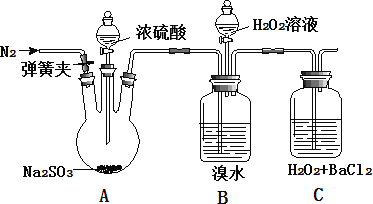
实验操作 | 实验现象 |
i. 打开 A 中分液漏斗活塞,滴加浓硫酸 | A 中有气泡产生,B 中红棕色褪色,C 中有白色沉淀 |
ii. 取 C 中沉淀加入盐酸 | C 中白色沉淀不溶解 |
iii. 打开B 中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加 H2O2 溶液,一段时间后,混合液逐渐变成红棕色 |
(1)A 中发生反应的化学方程式是_____。
(2)B 中红棕色褪色的离子方程式是_____。
(3)甲同学通过 C 中产生白色沉淀,得出结论,氧化性:H2O2>SO2。C 中产生白色沉淀的离子方程式是_____。
①乙同学认为不能得出此结论, 认为在滴加浓硫酸之前应增加一步操作, 该操作是_____。
②丙同学认为还应该在 B 和 C 之间增加洗气瓶 D,D 中盛放的试剂是_____。
③将乙和丙同学改进后的方案进行实验,C 中产生白色沉淀,得出结论:氧化性 H2O2>SO2。
(4)iii 中滴入少量 H2O2 没有明显变化。提出假设:
观点 1:H2O2 的量少不能氧化溴离子
观点 2:B 中有未反应 SO2
为验证观点 2,应进行的实验操作及现象是_____。
(5)通过上述全部实验,得出结论:H2O2、SO2、Br2 氧化性由强到弱的顺序是_____。