题目内容
下列有关说法不正确的是( )
| A、太阳能电池使用的材料主要是硅 |
| B、实验室可以用NaOH溶液处理SO2和NO2废气 |
| C、氯气具有很强的氧化性,在化学反应中只能作氧化剂 |
| D、用盐酸可以清洗长期存放过FeCl3溶液的试剂瓶 |
考点:硅和二氧化硅,氯气的化学性质,氮的氧化物的性质及其对环境的影响,二氧化硫的化学性质
专题:元素及其化合物
分析:A.晶体硅可导电;
B.SO2和NO2可与氢氧化钠溶液反应而被吸收;
C.氯气中Cl元素化合价为中间价态,既可被氧化,也可被还原;
D.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁,可与盐酸反应.
B.SO2和NO2可与氢氧化钠溶液反应而被吸收;
C.氯气中Cl元素化合价为中间价态,既可被氧化,也可被还原;
D.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁,可与盐酸反应.
解答:
解:A.晶体硅可导电,可用太阳能电池,故A正确;
B.SO2和NO2可与氢氧化钠溶液反应而被吸收,分别生成亚硫酸钠、硝酸钠、亚硝酸钠等物质,故B正确;
C.氯气中Cl元素化合价为中间价态,既可被氧化,也可被还原,如Cl2+H2O=HCl+HClO,反应中氯气既是氧化剂也是还原剂,故C错误;
D.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁,可与盐酸反应,故D正确.
故选C.
B.SO2和NO2可与氢氧化钠溶液反应而被吸收,分别生成亚硫酸钠、硝酸钠、亚硝酸钠等物质,故B正确;
C.氯气中Cl元素化合价为中间价态,既可被氧化,也可被还原,如Cl2+H2O=HCl+HClO,反应中氯气既是氧化剂也是还原剂,故C错误;
D.长期存放过FeCl3溶液的试剂瓶,表面残留氧化铁,可与盐酸反应,故D正确.
故选C.
点评:本题综合考查元素化合物知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,题目贴近高考,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
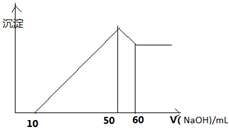 某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )
某溶液中含有H+、Al3+、Mg2+、Cu2+四种阳离子,且Mg2+ Cu2+物质的量之为1:1,逐滴加入0.1moL/L NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+、Cu2+四种阳离子的物质的量浓度之比为( )| A、1:1:1:1 |
| B、2:2:1:1 |
| C、2:1:1:1 |
| D、4:4:1:1 |
下列各对化合物中,化学键与晶体类型都相同的一组是( )
| A、H2S、HCl |
| B、NaCl、HF |
| C、SiO2、CO2 |
| D、CCl4、KCl |
Fe与HNO3反应随温度和HNO3的浓度不同而产物不同.已知0.2mol HNO3作氧化剂时,恰好把0.2mol Fe氧化,则HNO3可能被还原成( )
| A、NH4+ |
| B、NO2 |
| C、NO |
| D、N2O3 |
下列有关热化学方程式的叙述正确的是( )
| A、在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,若将含0.6mol H2SO4的稀硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、需要加热的反应说明它是吸热反应 |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
 M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图所示,则:
M元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图所示,则: