题目内容
13.下列除杂质的方法不可行的是( )| A. | 用过量氨水除去Al3+溶液中的少量Fe3+ | |
| B. | 将混合气体通过灼热的铜网除去N2中的少量O2 | |
| C. | 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 | |
| D. | 用饱和NaHCO3溶液除去混在H2中的HCl气体 |
分析 A.二者都与氨水反应生成沉淀;
B.加入条件下,氧气与铜反应;
C.水与氧化钙反应;
D.生成二氧化碳,引入新杂质.
解答 解:A.二者都与氨水反应生成沉淀,可加入氢氧化铝调节溶液pH,使铁离子水解生成氢氧化铁沉淀而除去,故A错误;
B.加入条件下,氧气与铜反应,可用于除杂,故B正确;
C.水与氧化钙反应生成氢氧化钙,蒸馏可得到乙醇,故C正确;
D.生成二氧化碳,引入新杂质,应用氢氧化钠溶液除杂,故D错误.
故选AD.
点评 本题考查物质的分离、提纯,为高频考点,侧重于学生的分析、实验能力的考查,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
3.如图是一原电池的装置,关于它的说法正确的是( )
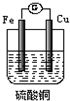

| A. | 装置中铜是负极 | |
| B. | 铜表面的反应为:2H++2e-=H2↑ | |
| C. | 电流的方向是从铁经导线流向铜 | |
| D. | 构成原电池后,铁与硫酸铜的反应速率加快 |
4.下列各组微粒,具有相同质子数和电子数的是( )
| A. | CH4、NH3、HF | B. | OH-、F-、NH3 | C. | H3O+、NH4+、Mg2+ | D. | O2-、OH-、NH2- |
1.下列关于元素周期表和元素周期律的说法不正确的是( )
| A. | 从氟到碘,其氢化物的稳定性逐渐减弱 | |
| B. | 因为铝原子比钠原子失去电子数目多,所以铝比钠的还原性强 | |
| C. | 第三周期从钠到氯,最高价氧化物的水化物碱性逐渐减弱,酸性逐渐增强 | |
| D. | 氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |
8.用石墨电极电解稀硫酸的过程中,溶液pH的变化情况为( )
| A. | 不改变 | B. | 逐渐减小 | C. | 逐渐增大 | D. | 先减小,后增大 |
18.质量相同的两份铝分别与100mL3mol/L的稀HCl溶液和100mL3mol/L的NaOH溶液反应,在同温、同压下产生的氢气体积之比为1:2,则加入铝粉的质量为( )
| A. | 1.8g | B. | 2.7g | C. | 3.6g | D. | 5.4g |
5.①Al ②Al2O3 ③Al(OH)3 ④NaHCO3,其中既能跟盐酸反应,又能跟NaOH反应是( )
| A. | ①②③ | B. | ①④ | C. | ①③ | D. | ①②③④ |
2.铜锌原电池(如图)工作时,下列叙述正确的是( )
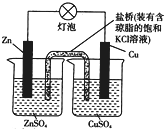

| A. | 正极反应为Zn-2e-═Zn2+ | B. | 电池反应为Zn2++Cu═Zn+Cu2+ | ||
| C. | 在外电路中,电子从负极流向正极 | D. | 盐桥中的K+移向ZnSO溶液 |
3.用氯化铝制取的纯净的硝酸铝的最佳方法是( )
| A. | 用氯化铝与纯硝酸反应 | |
| B. | 用氯化铝溶液和硝酸钡溶液反应 | |
| C. | 用氯化铝溶液与氢氧化钠反应,过滤得沉淀再加纯HNO3 | |
| D. | 用氯化铝溶液与氨水反应,过滤得沉淀再加纯HNO3 |