题目内容
4.下列各组微粒,具有相同质子数和电子数的是( )| A. | CH4、NH3、HF | B. | OH-、F-、NH3 | C. | H3O+、NH4+、Mg2+ | D. | O2-、OH-、NH2- |
分析 根据原子的质子数相加即为微粒的质子数,阴离子中,电子数=质子数+电荷数,阳离子中,电子数=质子数-电荷数来分析解答.
解答 解:A、CH4、NH3、HF的质子数分别为10,10、10,电子数分别为10,10、10,故A正确;
B、OH-、F-、NH3的质子数分别为9、9、10,电子数分别为10、10、10,故B错误;
C、H3O+、NH4+、Mg2+的质子数都是11、11、12电子数都是10,故C错误;
D、O2-、OH-、NH2-的质子数分别为8、9、9,电子数都是10,故D错误;
故选A.
点评 本题考查微粒的质子数和电子数,明确质子数和电子数的计算及中性微粒中质子数等于电子数是解答本题的关键.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
14.X、Y、Z、Q、M为常见的短周期元素,其原子序数依次增大.有关信息如下表:
(1)X的气态氢化物的大量生产曾经解决了地球上因粮食不足而导致的饥饿和死亡问题,请写出该气态氢化物的电子式 .
.
(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
| X | 动植物生长不可缺少的元素,是组成蛋白质的重要元素 |
| Y | 地壳中含量居第一位 |
| Z | 短周期中其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
 .
.(2)已知37Rb和53I都位于第五周期,分别与Z和M同一主族.下列有关说法正确的是ACD(填序号).
A.原子半径:Rb>I
B.RbM中含有共价键
C.气态氢化物热稳定性:M>I
D.Rb、Q、M的最高价氧化物对应的水化物可以两两发生反应
(3)若XM3最初水解产物是XH3和HMO,则X、M元素的电负性大小顺序是:X>M((填>、<、或=);若已知磷与M元素电负性关系是:P<M,则PM3水解的化学反应方程式是PCl3+3H2O=3HCl+H3PO3.
(4)X、Y组成的一种无色气体遇空气变为红棕色.将标准状况下40L该无色气体与15L氧气通入一定浓度的NaOH溶液中,恰好被完全吸收,同时生成两种盐.请写出该反应的离子方程式8NO+3O2+8OH-=2NO3-+6NO2-+4H2O.
15.下列化合物中,既可看作醇,又可看作酚的是( )
| A. | 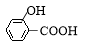 | B. | 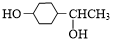 | C. | 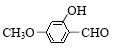 | D. | 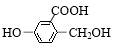 |
12.关于氢元素的叙述,不正确的是( )
| A. | 自然界中氢元素有三种同位素,它们的性质相同 | |
| B. | 三种同位素在化学反应中容易失去一个电子而呈+1价 | |
| C. | ${\;}_{1}^{1}$H原子失去一个电子后变成一个质子 | |
| D. | 氢在周期表中与碱金属同属ⅠA族 |
19.下列物质中属于含有极性键的非极性分子的是( )
| A. | CS2 | B. | H2O | C. | CH3CH2Cl | D. | NH3 |
16.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述不正确的是( )
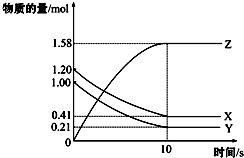

| A. | 反应开始到10s,用Z表示的反应速率为0.079mol/(L•s) | |
| B. | 该反应的方程式为:X(g)+Y(g)?2 Z(g) | |
| C. | 反应开始到10s时,Y的转化率为79.0% | |
| D. | 反应进行到10s时,该反应达到限度且各组分浓度相等 |
13.下列除杂质的方法不可行的是( )
| A. | 用过量氨水除去Al3+溶液中的少量Fe3+ | |
| B. | 将混合气体通过灼热的铜网除去N2中的少量O2 | |
| C. | 用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 | |
| D. | 用饱和NaHCO3溶液除去混在H2中的HCl气体 |
14.某学习小组欲用如图装置制取纯净干燥的氯气,并探究其性质.
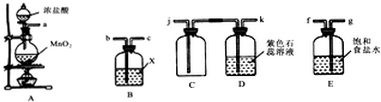
(1)装置A中发生反应的化学方程式为MnO2+4HCl(浓)═$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)欲制得干燥的氯气,B中广口瓶所装液体X为浓硫酸;
(3)欲收集纯净干燥的氯气并检验氯气部分性质,上述仪器接口的连接顺序为:
a→(g)→(f)→(b)→(c)→(j)→(k);
(4)连接好装置,将A中气体通入D中较长时间,可观察到的现象是石蕊试液先变红后褪色,最后呈浅黄绿色;
(5)实验设计及改进:利用制得的纯净干燥氯气,用下图装置证明Na2SO3具有还原性;同时对上述实验的不足进行改进.
试剂:Na2SO3溶液、Ba( NO3)2溶液、BaCl2溶液、稀盐酸、NaOH溶液、紫色石蕊溶液
试完成下列表格中的问题:

(1)装置A中发生反应的化学方程式为MnO2+4HCl(浓)═$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)欲制得干燥的氯气,B中广口瓶所装液体X为浓硫酸;
(3)欲收集纯净干燥的氯气并检验氯气部分性质,上述仪器接口的连接顺序为:
a→(g)→(f)→(b)→(c)→(j)→(k);
(4)连接好装置,将A中气体通入D中较长时间,可观察到的现象是石蕊试液先变红后褪色,最后呈浅黄绿色;
(5)实验设计及改进:利用制得的纯净干燥氯气,用下图装置证明Na2SO3具有还原性;同时对上述实验的不足进行改进.
试剂:Na2SO3溶液、Ba( NO3)2溶液、BaCl2溶液、稀盐酸、NaOH溶液、紫色石蕊溶液
试完成下列表格中的问题:
| 实验装置设计. | 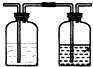 (注明所用试剂及气体流向) (注明所用试剂及气体流向)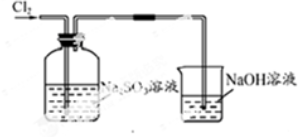 |
| 实验步驟及现象 | 连接好装置,将氯气通入亚硫酸钠溶液中,充分反应.取少量所得溶液与试管,滴入几滴氯化钡,有白色沉淀,再加入少量盐酸,沉淀不溶解. |
| 离子方程式 | Cl2+SO32-+H2O=2Cl-+SO42-+2H+; SO42-+Ba2+=BaSO4↓ |
| 结论 | Na2SO3具有还原性,能被氯气氧化成Na2SO4 |
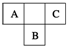 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.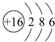 ,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).
,C的氢化物与B的氢化物的稳定性强弱顺序为HF>H2S(填化学式).