题目内容
16.用NA表示阿伏伽德罗常数,下列说法正确的是( )| A. | 用含0.1molFeCl3的溶液与足量沸水反应制得得Fe(OH)3胶体中胶粒数为0.1NA | |
| B. | 0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA | |
| C. | 将1mol氯气分别通入足量的FeBr2和FeI2溶液中转移电子数均为2NA | |
| D. | 等物质的量的NH4+和OH-含电子数均为10NA |
分析 A、一个氢氧化铁胶粒是多个氢氧化铁分子的聚集体;
B、氯气的量不足,根据氯气的物质的量计算转移电子数;
C、根据反应后氯元素的价态为-1价来分析;
D、NH4+和OH-的物质的量不明确.
解答 解:A、一个氢氧化铁胶粒是多个氢氧化铁分子的聚集体,故0.1mol氯化铁所制的氢氧化铁胶粒的个数小于0.1NA个,故A错误;
B、0.1 mol铁在0.1 mol Cl2中充分燃烧,氯气的物质的量不足,转移的电子的物质的量是0.2mol,有0.2NA个电子转移,故B错误;
C、由于反应后氯元素为-1价,故1mol氯气转移2mol电子即2NA个,故C正确;
D、NH4+和OH-的物质的量不明确,不一定是1mol,故含有的电子数不一定为10NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.下列粒子在反应中只能作氧化剂的是( )
| A. | O 2- | B. | Cl 2 | C. | HCl | D. | Fe 3+ |
4.草酸与高锰酸钾在酸性条件下能够发生如下反应:MnO4-+H2C2O4+H+═Mn2++CO2↑+H2O(未配平)用4mL 0.001mol•L-1KMnO4溶液与2mL 0.01mol•L-1H2C2O4溶液,研究不同条件对化学反应速率的影响.改变的条件如表:
(1)该反应中氧化剂和还原剂的物质的量之比为2:5.
(2)如果研究催化剂对化学反应速率的影响,使用实验Ⅰ和Ⅱ(用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验Ⅰ和Ⅲ.
(3)对比实验I和IV,可以研究浓度对化学反应速率的影响,实验IV中加入1mL蒸馏水的目的是确保所有实验中c(KMnO4)、c(H2C2O4)浓度不变和总体积不变.
| 实验 | 硫酸(10%)体积/mL | 温度/℃ | 其他物质 |
| I | 2mL | 20 | / |
| II | 2mL | 20 | 10滴饱和MnSO4溶液 |
| III | 2mL | 30 | / |
| IV | 1mL | 20 | 1mL蒸馏水 |
(2)如果研究催化剂对化学反应速率的影响,使用实验Ⅰ和Ⅱ(用I~IV表示,下同);如果研究温度对化学反应速率的影响,使用实验Ⅰ和Ⅲ.
(3)对比实验I和IV,可以研究浓度对化学反应速率的影响,实验IV中加入1mL蒸馏水的目的是确保所有实验中c(KMnO4)、c(H2C2O4)浓度不变和总体积不变.
11.用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,会引起滴定结果偏低的是( )
| A. | 用蒸馏水洗净滴定管后,装入标准盐酸进行滴定 | |
| B. | 用蒸馏水冼净锥形瓶后,再用NaOH液润洗,而后装入一定体积的NaOH溶液 | |
| C. | 滴定前平视滴定管刻度线,滴定终了俯视刻度线 | |
| D. | 滴定前酸式滴定管尖嘴部分有气泡,滴定终了无气泡 |
1.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 50g46%的乙醇水溶液中,含H原子总数目为3NA | |
| C. | 7.8gNa2O2加入足量的水中,反应转移的电子总数目为0.2NA | |
| D. | 常温,21.0g乙烯和环丙烯的混合气体中含有的碳原子数为1.5NA |
8.下列说法错误的是( )
| A. | s轨道呈球形,p轨道呈哑铃形 | B. | Cu元素在元素周期表的d区 | ||
| C. | 12g二氧化硅中有0.8NA个Si-O键 | D. | H2O中O原子的杂化方式是sp3 |
6.下列对实验事故或药品的处理方法正确的是( )
| A. | 实验台上的酒精灯被碰翻着火,立即用湿抹布扑灭 | |
| B. | 金属钠着火燃烧时,用泡沫灭火器扑灭 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氨水冲洗 | |
| D. | 将含硫酸的废液直接倒入水槽,用水冲入下水道 |
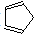 )合成二茂铁.环戊二烯中碳原子的杂化方式为sp2、sp3;1mol环戊二烯中含有的σ键数目为11NA.
)合成二茂铁.环戊二烯中碳原子的杂化方式为sp2、sp3;1mol环戊二烯中含有的σ键数目为11NA.