题目内容
【题目】根据下列图示所得出的结论一定错误的是
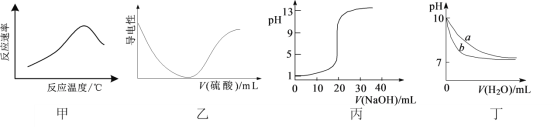
A.图甲表示酶催化反应的反应速率随反应温度的变化
B.图乙表示向BaCl2溶液中滴加稀硫酸至过量的过程中溶液导电性的变化
C.图丙表示用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1醋酸的滴定曲线
D.图丁表示相同温度下,向等体积pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线
【答案】C
【解析】
A. 酶为蛋白质,温度过高,蛋白质变性,则酶催化能力降低,甚至失去催化活性,图中能表示酶催化反应的反应速率随反应温度的变化,故A正确;
B. 向BaCl2溶液中滴加稀硫酸至过量,溶液导电性有所减弱,但不会接近0,图象曲线变化与实际不符,故B错误;
C.NaOH溶液体积为0时,溶液的pH=1,此时为醋酸溶液,由于醋酸为弱酸,则0.1000molL1醋酸溶液的pH>1,图象曲线变化与实际不符,故C错误;
D.pH=10的氢氧化钠溶液和氨水,稀释时一水合氨继续电离,则稀释时NaOH的pH变化大,所以a表示氨水稀释时pH的变化曲线,故D正确;
故答案选BC。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目