题目内容
【题目】如图为实验室某浓硫酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
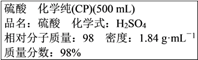
(1)通过计算可知,上述浓硫酸中H2SO4的物质的量浓度为__________molL-1。
实验室需要240 mL 2.0 mol·L-1的H2SO4溶液,现用以上浓硫酸配制,请回答下列问题:
(2)下列仪器中,不会用到的是________。
A.50 mL量筒 B.100 mL容量瓶 C.玻璃棒 D.托盘天平 E.药匙 F.烧杯
(3)若要实施配制,除上述仪器外,还缺少的仪器为________。
(4)请先通过计算____(请把计算过程写在框内),再确定量取________mL浓硫酸溶液用于稀释。
(5)配制过程简述为以下各步,其正确的操作顺序为_________________(填各步骤序号)。
A.冷却至室温 B.洗涤并移液 C.量取 D.稀释 E.摇匀装瓶 F.定容 G.移液
(6)在配制过程中,下列情况对配制结果有何影响?(填“偏高”“偏低”或“无影响”)
①容量瓶未干燥,有少量蒸馏水,则所配溶液的浓度________;
②定容时若仰视刻度线,则所配溶液的浓度________;
③量取浓硫酸时若俯视刻度线,则所配溶液的浓度________;
④摇匀后,发现液面低于刻度线,再加水至刻度线________。
【答案】 18.4 BDE 250mL容量瓶、胶头滴管 27.2mL 稀溶液有n=C稀V稀=2.0mol/L × 0.25L=0.5mol,浓溶液的体积V浓=n/C浓=0.5mol/18.4molL-1=27.2mL(保留一位小数才给分) CDAGBFE 无影响 偏低 偏低 偏低
【解析】(1)根据![]() 可知该浓硫酸的物质的量浓度为:
可知该浓硫酸的物质的量浓度为: ![]() ;(2)没有240mL容量瓶,需要配制250mL溶液,需要硫酸的物质的量为:2.0mol/L×0.25L=0.5mol,配制过程中硫酸的物质的量不变,则需要18.4mol/L的浓硫酸的体积为:0.5mol÷18.4mol/L≈0.02717L=27.2mL,因此需要50mL量筒。配制溶液的一般步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶、贴标签,需要的仪器为:量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,所以不需要的是BDE;(3)根据以上分析可知还缺少的仪器为250mL容量瓶和胶头滴管;(4)根据以上分析可知需要浓硫酸的体积是27.2mL;(5)根据以上分析可知正确的操作顺序为CDAGBFE;(6)①容量瓶未干燥,有少量蒸馏水,不会影响;②定容时若仰视刻度线,液面在刻度线上方,则所配溶液的浓度偏低;③量取浓硫酸时若俯视刻度线,量取的浓硫酸体积减少,则所配溶液的浓度偏低;④摇匀后,发现液面低于刻度线,再加水至刻度线,溶液体积增加,浓度偏低。
;(2)没有240mL容量瓶,需要配制250mL溶液,需要硫酸的物质的量为:2.0mol/L×0.25L=0.5mol,配制过程中硫酸的物质的量不变,则需要18.4mol/L的浓硫酸的体积为:0.5mol÷18.4mol/L≈0.02717L=27.2mL,因此需要50mL量筒。配制溶液的一般步骤为:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶、贴标签,需要的仪器为:量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,所以不需要的是BDE;(3)根据以上分析可知还缺少的仪器为250mL容量瓶和胶头滴管;(4)根据以上分析可知需要浓硫酸的体积是27.2mL;(5)根据以上分析可知正确的操作顺序为CDAGBFE;(6)①容量瓶未干燥,有少量蒸馏水,不会影响;②定容时若仰视刻度线,液面在刻度线上方,则所配溶液的浓度偏低;③量取浓硫酸时若俯视刻度线,量取的浓硫酸体积减少,则所配溶液的浓度偏低;④摇匀后,发现液面低于刻度线,再加水至刻度线,溶液体积增加,浓度偏低。