题目内容
【题目】海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
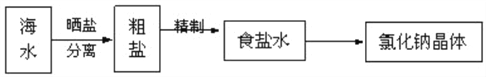
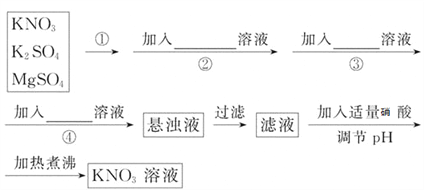
粗盐中含Ca2+、Mg2+、Fe3+、SO42﹣等杂质,提纯的步骤有:①加入过量的Na2CO3溶液;
②加入过量的BaCl2溶液; ③加入过量的NaOH溶液;④加入适量盐酸; ⑤溶解; ⑥过滤; ⑦蒸发.其正确的操作顺序是( )
A. ⑤①③②⑥④⑦ B. ⑤①②③⑥④⑦ C. ⑤②①③④⑥⑦ D. ⑤③②①⑥④⑦
【答案】D
【解析】粗盐中含Ca2+、Mg2+、Fe3+、SO42-等杂质,提纯过程中,先加水溶解,然后把杂质转化为沉淀或气体除去,除Ca2+用CO32-,除Mg2+、Fe3+用OH-,除SO42-用Ba2+,要注意后加的试剂最好能把前面先加的过量试剂除掉,所以先加过量的NaOH溶液除去Mg2+、Fe3+,再加加入过量的BaCl2溶液除去SO42-,然后加过量的Na2CO3溶液除去Ca2+和过量的Ba2+,过滤出沉淀后加入适量盐酸除去CO32-,最后蒸发结晶,故其正确的操作顺序是⑤③②①⑥④⑦,选D。

练习册系列答案
相关题目
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸产生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应