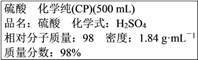题目内容
【题目】(12分)
SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
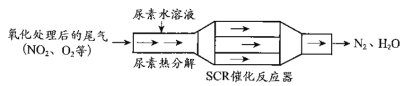
① 尿素[CO(NH2)2]水溶液热分解为NH3和CO2,该反应的化学方程式:____________。
② 反应器中NH3还原CO2的化学方程式:____________。
③ 当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:________。
④ 尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60 mg·L1)含量的方法如下:取a g尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1 mL c1 mol·L1 H2SO4溶液吸收完全,剩余H2SO4用v2 mL c2 mol·L1 NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是_________。
(2)NSR(NOx储存还原)工作原理:
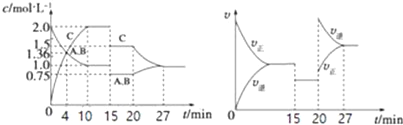
NOx的储存和还原在不同时段交替进行,如图a所示。
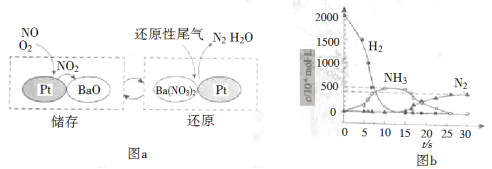
① 通过BaO和Ba(NO3)2的相互转化实验NOx的储存和还原。储存NOx的物质是_________。
② 用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__________。
③ 还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:_______![]() □15NNO+□H2O
□15NNO+□H2O
【答案】
(1)①CO(NH2)2+H2O![]() 2NH3↑+CO2↑ ②8NH3+6NO2
2NH3↑+CO2↑ ②8NH3+6NO2![]() 7N2+12H2O ③2SO2+O2+4NH3+2H2O==2(NH4)2SO4 ④
7N2+12H2O ③2SO2+O2+4NH3+2H2O==2(NH4)2SO4 ④![]() (2)①BaO ②8∶1 ③415NO+4NH3+3O2
(2)①BaO ②8∶1 ③415NO+4NH3+3O2![]() 415NNO+6H2O
415NNO+6H2O
【解析】(1)①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,结合原子守恒,发生反应的化学方程式为CO(NH2)2+H2O![]() 2NH3↑+CO2↑.。正确答案:①CO(NH2)2+H2O
2NH3↑+CO2↑.。正确答案:①CO(NH2)2+H2O![]() 2NH3↑+CO2↑。②从图中可以看出NH3在催化剂作用下还原NO2生成氮气和水,根据电子守恒和原子守恒可得此反应的化学方程式为8NH3+6NO2
2NH3↑+CO2↑。②从图中可以看出NH3在催化剂作用下还原NO2生成氮气和水,根据电子守恒和原子守恒可得此反应的化学方程式为8NH3+6NO2![]() 7N2+12H2O。正确答案:8NH3+6NO2
7N2+12H2O。正确答案:8NH3+6NO2![]() 7N2+12H2O。③SO2在O2作用下与NH3、H2O反应形成(NH4)2SO4,此反应中SO2是还原剂,氧气是氧化剂,结合电子守恒和原子守恒可得此反应的化学方程式为2SO2+O2+4NH3+2H2O==2(NH4)2SO4。正确答案:2SO2+O2+4NH3+2H2O==2(NH4)2SO4。④吸收NH3的硫酸的物质的量为v1×10-3L× c1 mol·L1 -v2 ×10-3L×c2 mol·L1 ×
7N2+12H2O。③SO2在O2作用下与NH3、H2O反应形成(NH4)2SO4,此反应中SO2是还原剂,氧气是氧化剂,结合电子守恒和原子守恒可得此反应的化学方程式为2SO2+O2+4NH3+2H2O==2(NH4)2SO4。正确答案:2SO2+O2+4NH3+2H2O==2(NH4)2SO4。④吸收NH3的硫酸的物质的量为v1×10-3L× c1 mol·L1 -v2 ×10-3L×c2 mol·L1 ×![]() =(v1c1-
=(v1c1-![]() v2c2)×10-3mol,尿素的物质的量为(v1c1-
v2c2)×10-3mol,尿素的物质的量为(v1c1-![]() v2c2)×10-3mol,则尿素溶液中溶质的质量分数是[(v1c1-
v2c2)×10-3mol,则尿素溶液中溶质的质量分数是[(v1c1-![]() v2c2)×10-3mol×60g/mol]÷a g×100%=
v2c2)×10-3mol×60g/mol]÷a g×100%=![]() 。正确答案:
。正确答案:![]() 。(2)①由图示可知BaO和NOx作用生成Ba(NO3)2,Ba(NO3)
。(2)①由图示可知BaO和NOx作用生成Ba(NO3)2,Ba(NO3)![]() 415NNO+6H2O。正确答案:415NO+4NH3+3O2
415NNO+6H2O。正确答案:415NO+4NH3+3O2![]() 415NNO+6H2O。
415NNO+6H2O。

 53随堂测系列答案
53随堂测系列答案