题目内容
已知氢氧化镁饱和溶液中存在下列平衡:Mg(OH)2(s)
 Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)某同学在t℃(室温)下用纯水制备了一份氢氧化镁饱和溶液,测得溶液的pH为10。
(1)用上述测定数据计算在t℃时氢氧化镁的溶解度(用mol?L-1单位表示)。
(2)计算在t℃时氢氧化镁的Ksp。
见分析
【试题分析】
这是一道以沉淀溶解平衡为背景命制的试题,涉及到Ksp的有关运算。(1)由题意知c(OH-)=10-4mol?L-1,故c(Mg2+)=5×10-5mol/L,则t℃时其溶解度就是5×10-5mol/L。(2)Ksp=c(Mg2+)?c2(OH-)=5×10-5×(10-4)2=5×10-13。

练习册系列答案
相关题目
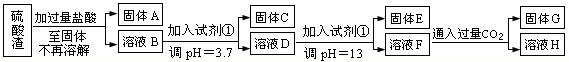
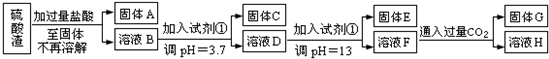
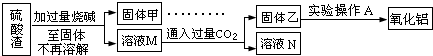
硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。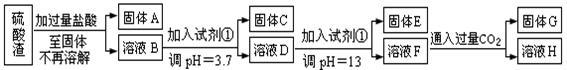
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
(4)H中溶质的化学式: ;
(5)计算溶液F中c(Mg2+)= ( 25℃时,氢氧化镁的Ksp=5.6×10-12)