题目内容
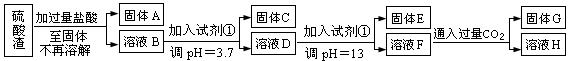
硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO.某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验.

已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol?L-1.请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式:
(2)上述流程中两次使用试剂①,推测试剂①应该是
A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是
(4)固体E为
(5)计算溶液F中c(Mg2+)=

已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol?L-1.请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式:
SiO2+2NaOH=Na2SiO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
.(2)上述流程中两次使用试剂①,推测试剂①应该是
A
A
(填以下字母编号)A.氢氧化钠 B.氧化铝 C.氨水 D.水
(3)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是
镁离子沉淀不完全或氢氧化铝溶解不完全等
镁离子沉淀不完全或氢氧化铝溶解不完全等
;(任写一点)(4)固体E为
Mg(OH)2
Mg(OH)2
,写出溶液F通入过量CO2生成固体G和溶液H的化学方程式:NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3
NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3
.(5)计算溶液F中c(Mg2+)=
5.6×10-10mol/L
5.6×10-10mol/L
(25℃时,氢氧化镁的Ksp=5.6×10-12)分析:先判断各物质的组成,在根据题目要求分析该题.
硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量盐酸时,二氧化硅和盐酸不反应,所以固体A是二氧化硅,氧化铁、氧化铝、氧化镁和盐酸反应,所以溶液B的溶质是氯化镁、氯化铁、氯化铝、盐酸;向溶液B中加试剂①并调节溶液的PH值为3.7,结合题意溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,固体C是氢氧化铁;向溶液D中加入试剂①并调节溶液的PH值为13,溶液呈强碱性溶液,铝元素在溶液中以偏铝酸根离子存在,镁离子和氢氧根离子生成氢氧化镁沉淀,所以固体E是氢氧化镁;溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,所以G是氢氧化铝.
(1)根据二氧化硅和氢氧化钠的性质写出相应的化学反应方程式.
(2)能使铁离子产生沉淀,而铝离子不产生沉淀的物质只能是强碱.
(3)在强碱性条件下,铝元素以偏铝酸根离子存在,镁元素以氢氧化镁存在,据此分析.
(4)氢氧化铝的酸性比碳酸还弱,根据强酸制取弱酸知,偏铝酸钠和过量二氧化碳能反应生成氢氧化铝和碳酸氢钠.
(5)根据c(Mg2+)=
计算.
硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量盐酸时,二氧化硅和盐酸不反应,所以固体A是二氧化硅,氧化铁、氧化铝、氧化镁和盐酸反应,所以溶液B的溶质是氯化镁、氯化铁、氯化铝、盐酸;向溶液B中加试剂①并调节溶液的PH值为3.7,结合题意溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,固体C是氢氧化铁;向溶液D中加入试剂①并调节溶液的PH值为13,溶液呈强碱性溶液,铝元素在溶液中以偏铝酸根离子存在,镁离子和氢氧根离子生成氢氧化镁沉淀,所以固体E是氢氧化镁;溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,所以G是氢氧化铝.
(1)根据二氧化硅和氢氧化钠的性质写出相应的化学反应方程式.
(2)能使铁离子产生沉淀,而铝离子不产生沉淀的物质只能是强碱.
(3)在强碱性条件下,铝元素以偏铝酸根离子存在,镁元素以氢氧化镁存在,据此分析.
(4)氢氧化铝的酸性比碳酸还弱,根据强酸制取弱酸知,偏铝酸钠和过量二氧化碳能反应生成氢氧化铝和碳酸氢钠.
(5)根据c(Mg2+)=
| Ksp |
| C(OH-)2 |
解答:解:硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量盐酸时,二氧化硅和盐酸不反应,所以固体A是二氧化硅,氧化铁、氧化铝、氧化镁和盐酸反应,所以溶液B的溶质是氯化镁、氯化铁、氯化铝、盐酸;向溶液B中加试剂①并调节溶液的PH值为3.7,结合题意溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,固体C是氢氧化铁;向溶液D中加入试剂①并调节溶液的PH值为13,溶液呈强碱性溶液,铝元素在溶液中以偏铝酸根离子存在,镁离子和氢氧根离子生成氢氧化镁沉淀,所以固体E是氢氧化镁;溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,所以G是氢氧化铝.
(1)通过以上分析知,A是二氧化硅,二氧化硅是酸性氧化物,能和强碱反应生成盐和水,
所以反应方程式为:SiO2+2NaOH=Na2SiO3+H2O.
故答案为:SiO2+2NaOH=Na2SiO3+H2O.
(2)向溶液B中加试剂①并调节溶液的PH值为3.7,结合题意知,溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,符合条件的是A选项.
故选A.
(3)在强碱性条件下,铝元素以偏铝酸根离子存在,镁元素以氢氧化镁存在,当溶液的PH=13时,溶液呈强碱性,如果pH过小,可能导致的后果是镁离子沉淀不完全或氢氧化铝溶解不完全等.
故答案为:镁离子沉淀不完全或氢氧化铝溶解不完全等.
(4)通过以上分析知,固体E为Mg(OH)2,氢氧化铝的酸性比碳酸还弱,根据强酸制取弱酸知,偏铝酸钠和过量二氧化碳能反应生成氢氧化铝和碳酸氢钠,反应方程式为 NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3.
故答案为:Mg(OH)2;NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3.
(5)c(Mg2+)=
=
mol/L=5.6×10-10 mol/L
故答案为:5.6×10-10 mol/L.
(1)通过以上分析知,A是二氧化硅,二氧化硅是酸性氧化物,能和强碱反应生成盐和水,
所以反应方程式为:SiO2+2NaOH=Na2SiO3+H2O.
故答案为:SiO2+2NaOH=Na2SiO3+H2O.
(2)向溶液B中加试剂①并调节溶液的PH值为3.7,结合题意知,溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,符合条件的是A选项.
故选A.
(3)在强碱性条件下,铝元素以偏铝酸根离子存在,镁元素以氢氧化镁存在,当溶液的PH=13时,溶液呈强碱性,如果pH过小,可能导致的后果是镁离子沉淀不完全或氢氧化铝溶解不完全等.
故答案为:镁离子沉淀不完全或氢氧化铝溶解不完全等.
(4)通过以上分析知,固体E为Mg(OH)2,氢氧化铝的酸性比碳酸还弱,根据强酸制取弱酸知,偏铝酸钠和过量二氧化碳能反应生成氢氧化铝和碳酸氢钠,反应方程式为 NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3.
故答案为:Mg(OH)2;NaAlO2+CO2+H2O=Al(OH)3↓+NaHCO3.
(5)c(Mg2+)=
| Ksp |
| C(OH-)2 |
| 5.6×10-12 |
| (0.1)2 |
故答案为:5.6×10-10 mol/L.
点评:本题考查了物质的分离、提纯的方法选择及应用,难度不大,明确各物质的性质是解本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(每空3分共计10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。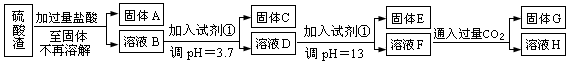
已知溶液pH=3.7时,Fe3+已经沉淀完全;一水合氨电离常数Kb=1.8×10-5,其饱和溶液中c(OH-)约为1×10-3mol·L-1。请回答:
(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中两次使用试剂①,推测试剂①应该是 (填以下字母编号)
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
(4)H中溶质的化学式: ;
(5)计算溶液F中c(Mg2+)= (25℃时,氢氧化镁的Ksp=5.6×10-12)
(10分)硫酸工业中废渣称为硫酸渣,其成分为SiO2、Fe2O3、Al2O3、MgO。某探究性学习小组的同学设计以下方案,进行硫酸渣中金属元素的提取实验。 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
请回答:(1)写出A与氢氧化钠溶液反应的化学方程式: 。
(2)上述流程中试剂②应该是 (填以下字母编号)。
| A.氢氧化钠 | B.氧化铝 | C.氨水 | D.水 |
。
(4)计算溶液F中c(Mg2+)= ( 25℃时,氢氧化镁的Ksp=5.6×10-12)。
(5)工业生产中将固体C灼烧后的产物与KNO3、KOH固体加热共熔制备净水剂K2FeO4,同时获得一种亚硝酸盐,请写出制得K2FeO4的化学方程式: 。
 已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。
已知:①Fe3+、Al3+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2和12.4;Al(OH)3完全溶解的pH为11.8。②常温下,饱和氨水的pH约为11。