题目内容
(10分)某化学兴趣小组利用浓盐酸、二氧化锰共热制氯气,并用氯气和消石灰制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 = Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应。试回答以下问题:
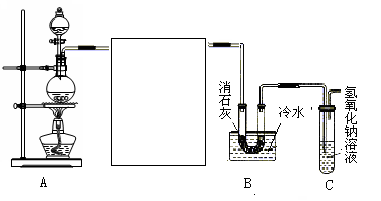
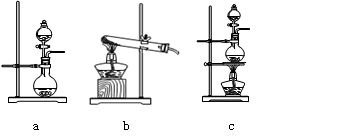
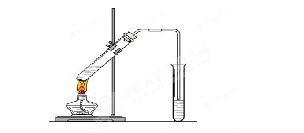
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式 。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内(示意图),并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是 。
(3)实验室若用16 mol ?L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过 mol。

(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过 (填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式 。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内(示意图),并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是 。
(3)实验室若用16 mol ?L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过 mol。
(每空2)(1)分液漏斗,MnO2 + 4H+ + 2Cl-(浓) Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O
(2)
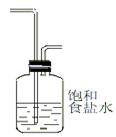
HCl会与Ca(OH)2和Ca(ClO) 2反应,影响产品质量。
(3)0.2 mol
 Mn2+ + Cl2↑+ 2H2O
Mn2+ + Cl2↑+ 2H2O(2)

HCl会与Ca(OH)2和Ca(ClO) 2反应,影响产品质量。
(3)0.2 mol
(1)根据装置图可知,盛放浓盐酸的仪器是分液漏斗。浓盐酸和二氧化锰反应的方程式为MnO2 + 4H+ + 2Cl-(浓) Mn2+ + Cl2↑+ 2H2O。
Mn2+ + Cl2↑+ 2H2O。
(2)由于浓盐酸具有挥发性,所以生成的氯气中混有氯化氢,而氯化氢能与Ca(OH)2和Ca(ClO) 2反应,影响产品质量,所以需要利用饱和食盐水除去氯气的氯化氢。
(3)16 mol ?L-1的盐酸100 mL的物质的量是1.6mol,所以根据方程式可知,生成氯气是0.4mol。氯气和氢氧化钙反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,所以理论上可以生成次氯酸钙0.2mol。
 Mn2+ + Cl2↑+ 2H2O。
Mn2+ + Cl2↑+ 2H2O。(2)由于浓盐酸具有挥发性,所以生成的氯气中混有氯化氢,而氯化氢能与Ca(OH)2和Ca(ClO) 2反应,影响产品质量,所以需要利用饱和食盐水除去氯气的氯化氢。
(3)16 mol ?L-1的盐酸100 mL的物质的量是1.6mol,所以根据方程式可知,生成氯气是0.4mol。氯气和氢氧化钙反应的方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,所以理论上可以生成次氯酸钙0.2mol。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
 2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。
2CaSO4+2Cl2↑+2H2O。某学习小组利用此原理设计如图所示装置制取氯气并探究其性质。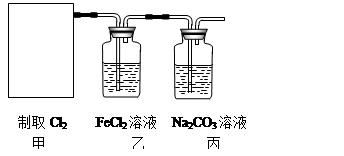
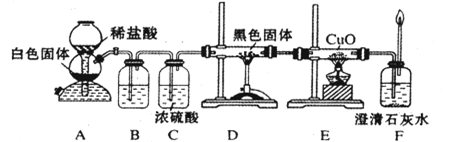
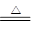 CO+H2 CO + H2O
CO+H2 CO + H2O 2CO
2CO 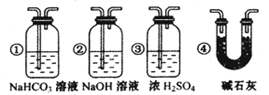

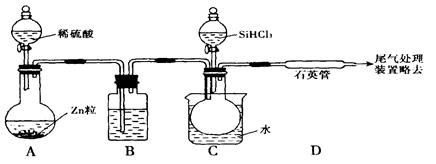
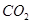 发生装置(X)的气密性,请写出主要操作过程:
发生装置(X)的气密性,请写出主要操作过程: SiHCl3 + H2(g)
SiHCl3 + H2(g) Si(s)+ 3HCl(g)
Si(s)+ 3HCl(g)