题目内容
2.对于反应A(g)+3B(g)?2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的速率,其中最快的是( )| A. | v(D)=0.4mol/(L•S) | B. | v(C)=0.5mol/(L•S) | C. | v(B)=0.6mol/(L•S) | D. | v(A)=0.15mol/(L•S) |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意单位保持一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,
A.$\frac{v(D)}{2}$=0.2mol/(L•min),
B.$\frac{v(C)}{2}$=0.25mol/(L•min);
C.$\frac{v(B)}{3}$=0.2mol/(L•min);
D.$\frac{v(A)}{1}$=0.15mol/(L•min);
故反应速率v(C)>v(D)=v(B)>v(A),
故选B.
点评 本题考查化学反应速率快慢比较,相同条件下同一反应中不同物质表示的速率大小可能不同,但表示的快慢是一样的,利用比值法可以迅速判断,也转化为同一物质表示的速率进行比较,注意保持单位一致.

练习册系列答案
相关题目
12.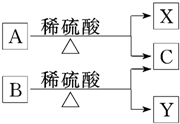 有机物A与B是分子式为C5H10O2的同分异构体,在酸性条件下均可水解,水解产物如图所示,下列有关说法中正确的是( )
有机物A与B是分子式为C5H10O2的同分异构体,在酸性条件下均可水解,水解产物如图所示,下列有关说法中正确的是( )
 有机物A与B是分子式为C5H10O2的同分异构体,在酸性条件下均可水解,水解产物如图所示,下列有关说法中正确的是( )
有机物A与B是分子式为C5H10O2的同分异构体,在酸性条件下均可水解,水解产物如图所示,下列有关说法中正确的是( )| A. | X、Y互为同系物 | B. | C分子中的碳原子最多有3个 | ||
| C. | X、Y化学性质不可能相似 | D. | X、Y一定互为同分异构体 |
13.设阿伏伽德罗常数为NA,则下列说法正确的是( )
| A. | 常温下,2.7g铝与足量的氢氧化钠溶液反应失去的电子数为0.1NA | |
| B. | 100mL1mol/LNa2SO4溶液中含Na+个数为0.1NA | |
| C. | 1.7gNH3中含电子数为NA | |
| D. | 11.2gCO2与8.5gNH3所含分子数都是0.5NA |
17.几种短周期元素的原子半径及主要化合价见表:根据表中信息,判断以下说法正确的是( )
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.111 | 0.104 | 0.143 | 0.066 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A. | 离子的还原性:T2->Z2- | |
| B. | 离子半径:Z2->X2+ | |
| C. | Y的原子序数大于X | |
| D. | X和Y的最高价氧化物的水化物的碱性:Y>X |
7.某金属A不溶于冷的浓硝酸,A与银用导线连接后浸入硫酸溶液,所组成的原电池中电流由银极通过导线流回A极,则A可能是( )
| A. | Pt | B. | Cu | C. | Zn | D. | Al |
14.下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑦是什么元素Al(用元素符号表示).
(2)请写出⑨的原子结构示意图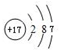 .
.
(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式: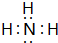
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
(2)请写出⑨的原子结构示意图
 .
.(3)②、③、④、⑤的半径从大到小的顺序是C>N>O>F(用元素符号表示).
(4)⑥与⑦两种元素金属性强弱顺序为:⑥>⑦(填“>”或“<”或“=”)
(5)①与③形成的最简单化合物的电子式:
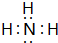
(6)请写出⑧元素最高价氧化物的化学式:SO3.⑥的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物相互反应的化学方程式:Al(OH)3+NaOH=NaAlO2+2H2O.
11.叶蝉散(isoprocard)对水稻叶蝉和飞虱具有较强的触杀作用,且残毒低.工业上用邻异丙基苯酚合成叶蝉散的过程如图:以下推断正确的是( )
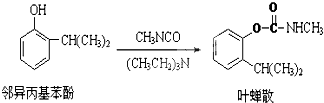

| A. | 邻异丙基苯酚发生了加成反应 | |
| B. | 邻异丙基苯酚发生了取代反应 | |
| C. | 除去叶蝉散中的邻异丙基苯酚可选用NaOH(aq) | |
| D. | 叶蝉散中是否含邻异丙基苯酚可用少量稀溴水检验 |
5.五种短周期主族元素如图所示,下列不正确的是( )
| X | L | Z |
| Y | W |
| A. | Y的原子半径一定比L的大 | |
| B. | 若X、Y为非金属元素,则X、Y元素形成的单质晶体类型一定相同 | |
| C. | 若X、W能组成XW型分子,则其空间构型分子,则其空间构型一定为直线型 | |
| D. | 对应简单氢化物的沸点可能是X>Y、Z>W |