题目内容
7.某金属A不溶于冷的浓硝酸,A与银用导线连接后浸入硫酸溶液,所组成的原电池中电流由银极通过导线流回A极,则A可能是( )| A. | Pt | B. | Cu | C. | Zn | D. | Al |
分析 某金属A不溶于冷的浓硝酸,说明A能发生钝化现象,A与银用导线连接后浸入硫酸溶液,所组成的原电池中电流由银通过导线流回A极,说明A的活动性大于Ag,据此分析解答.
解答 解:某金属A不溶于冷的浓硝酸,说明A能发生钝化现象,能发生钝化现象的有Al、Fe;A与银用导线连接后浸入硫酸溶液,所组成的原电池中电流由银通过导线流回A极,说明A的活动性大于Ag,Al和Fe活动性都大于Ag,则A可能是Fe或Al,故选D.
点评 本题考查钝化现象、原电池原理,知道钝化原理、原电池中金属活泼性强弱判断即可解答,注意:钝化现象不是不发生反应,为易错点.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
17.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 在密闭容器中加入1.5 mol H2和0.5 molN2,充分反应后可得到NH3分子数为NA | |
| C. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为6NA | |
| D. | 标准状况下,22.4 L的CCl4中C-Cl键数为4NA |
18.关于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在非金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 在地球上元素的分布和它们在元素周期表中的位置有密切关系 |
15.已知反应X+Y=M+N为放热反应,下列说法正确的是( )
| A. | X的能量不一定高于M的能量 | |
| B. | X和Y的总能量一定低于M和N的总能量 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | 此反应符合质量守恒,却不符合能量守恒 |
2.对于反应A(g)+3B(g)?2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的速率,其中最快的是( )
| A. | v(D)=0.4mol/(L•S) | B. | v(C)=0.5mol/(L•S) | C. | v(B)=0.6mol/(L•S) | D. | v(A)=0.15mol/(L•S) |
12.下列反应的离子方程式正确的是( )
| A. | NaHCO3溶液与盐酸:CO32-+2 H+=H2O+CO2↑ | |
| B. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag | |
| C. | 金属钾与水反应:K+H2O═K++OH-+H2↑ | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑ |
19.下列分子中,属于非极性分子的是( )
| A. | SO2 | B. | H2S | C. | BBr3 | D. | COCl2 |
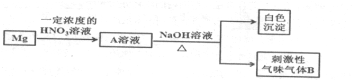
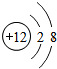 ;
;