题目内容
13.设阿伏伽德罗常数为NA,则下列说法正确的是( )| A. | 常温下,2.7g铝与足量的氢氧化钠溶液反应失去的电子数为0.1NA | |
| B. | 100mL1mol/LNa2SO4溶液中含Na+个数为0.1NA | |
| C. | 1.7gNH3中含电子数为NA | |
| D. | 11.2gCO2与8.5gNH3所含分子数都是0.5NA |
分析 A.铝为3价金属,2.7g铝的物质的量为0.1mol,完全反应0.1mol铝失去0.3mol电子;
B.Na2SO4中含有2个钠离子;
C.氨气分子中含有10个电子,1.7g氨气的物质的量为0.1mol,含有1mol电子;
D.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算二氧化碳的物质的量.
解答 解:A.2.7g铝的物质的量为$\frac{2.7g}{27g/mol}$=0.1mol,0.1mol铝完全反应失去0.3mol电子,失去的电子数为0.3NA,故A错误;
B.100mL1mol/LNa2SO4溶液中含Na+个数为0.1L×1mol/L×2=0.2mol,即0.2NA个,故B错误;
C.1.7g氨气的物质的量为$\frac{1.7g}{17g/mol}$=0.1mol,0.1mol氨气含有的电子数为0.1mil×10=1mol,即NA个,故C正确;
D.不是标况下,无法计算11.2L二氧化碳的物质的量,故D错误;
故选C.
点评 本题考查阿伏伽德罗常数的应用及计算,难度中等.注意明确标况下气体摩尔体积的使用条件.

练习册系列答案
相关题目
3.仅改变下列一个条件,通过提高活化分子的百分率来提高反应速率的是( )
| A. | 加热 | B. | 加压 | C. | 加负催化剂 | D. | 加大反应物浓度 |
4.某元素X的氢化物的化学式为H2X,则X的最高氧化物的水化物的化学式为( )
| A. | H2XO3 | B. | HXO3 | C. | H3XO4 | D. | H2XO4 |
1.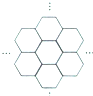 据报道,科学家己经研制出世界上最薄的材料一碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
据报道,科学家己经研制出世界上最薄的材料一碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
 据报道,科学家己经研制出世界上最薄的材料一碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
据报道,科学家己经研制出世界上最薄的材料一碳膜片,其厚度只有一根头发的二十万分之一.如图所示,这种碳膜片状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )| A. | 碳膜片属于单质 | |
| B. | 碳膜片与C60是同一种物质 | |
| C. | 碳膜片属于人工合成的有机高分子材料 | |
| D. | 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同 |
8.区别棉花和羊毛最简便的方法是( )
| A. | 加稀硫酸水解 | B. | 浸入水中 | C. | 加入碘水 | D. | 火上灼烧闻气味 |
18.关于元素周期表,下列叙述中不正确的是( )
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在非金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 在地球上元素的分布和它们在元素周期表中的位置有密切关系 |
5.分子式为C7H2402的有机物Q,在稀硫酸存在下能发生反应生成M、N,其中M的相对分子质量为60,下列有关说法中一定正确的是( )
| A. | Q可能有8种同分异构体 | B. | Q不可能有4种同分异构体 | ||
| C. | N只有2种同分异构体 | D. | M只有4种同分异构体 |
2.对于反应A(g)+3B(g)?2C(g)+2D(g),下列四个数据是在不同条件下测出的该反应的速率,其中最快的是( )
| A. | v(D)=0.4mol/(L•S) | B. | v(C)=0.5mol/(L•S) | C. | v(B)=0.6mol/(L•S) | D. | v(A)=0.15mol/(L•S) |
3.下列试剂能用于鉴别甲烷和乙烯的是( )
| A. | 溴水 | B. | 碳酸钠溶液 | C. | 酒精溶液 | D. | 四氯化碳 |