��Ŀ����
��һ�������������Ժ�CO2������Ӧ��Fe(s)+CO2(g) FeO(s)+CO(g) ��H>0��
FeO(s)+CO(g) ��H>0��
(1)���д�ʩ����ʹƽ��ʱc(CO)/c(CO2)������� (�����)��
A.�����¶� B.����ѹǿ
C.����һ�������� D.�ټ���һЩ����
(2)��Ӧ�ﵽƽ��������������������ʱ����ͨ��һ������CO2��ʹCO2��Ũ�ȳ�Ϊԭ����2������CO2��ת���ʽ� (���������С�����䡱)��
����һ���¶��µ�ij�ݻ��ɱ���ܱ������У��������л�ѧƽ�⣺C(s)+H2O(g) CO(g)+H2(g)���Է����ͻش��������⣺
CO(g)+H2(g)���Է����ͻش��������⣺
(1)���϶��������淴Ӧ��һ���������Ѵﵽ��ѧƽ��״̬���� (ѡ�����)��
A����ϵ��ѹǿ���ٷ����仯
B��v��(CO)=v��(H2O)
C������n mol CO��ͬʱ����n mol H2
D��1 mol H��H�����ѵ�ͬʱ����2 mol H��O��
(2)��������ѧƽ��״̬������Ӧ��ʼ�������ﵽƽ���ƽ����ϵ��ѹ(��С�ݻ���������������)���������������ƽ����Է��������� (��д�����䡱������С�����)��
 FeO(s)+CO(g) ��H>0��
FeO(s)+CO(g) ��H>0��(1)���д�ʩ����ʹƽ��ʱc(CO)/c(CO2)������� (�����)��
A.�����¶� B.����ѹǿ
C.����һ�������� D.�ټ���һЩ����
(2)��Ӧ�ﵽƽ��������������������ʱ����ͨ��һ������CO2��ʹCO2��Ũ�ȳ�Ϊԭ����2������CO2��ת���ʽ� (���������С�����䡱)��
����һ���¶��µ�ij�ݻ��ɱ���ܱ������У��������л�ѧƽ�⣺C(s)+H2O(g)
 CO(g)+H2(g)���Է����ͻش��������⣺
CO(g)+H2(g)���Է����ͻش��������⣺(1)���϶��������淴Ӧ��һ���������Ѵﵽ��ѧƽ��״̬���� (ѡ�����)��
A����ϵ��ѹǿ���ٷ����仯
B��v��(CO)=v��(H2O)
C������n mol CO��ͬʱ����n mol H2
D��1 mol H��H�����ѵ�ͬʱ����2 mol H��O��
(2)��������ѧƽ��״̬������Ӧ��ʼ�������ﵽƽ���ƽ����ϵ��ѹ(��С�ݻ���������������)���������������ƽ����Է��������� (��д�����䡱������С�����)��
��(1)A (2)���� ��(1)B��D (2)���
������Ҫע���������㣺
(1)����CO��CO2��Ũ�ȱ�ֵ��ϵ�ó�ƽ���ƶ��ķ���Ȼ���ٽ����жϡ�
(2)����Ӧ���Ũ�ȣ���Ӧ���ת���ʲ�һ����С��ת���ʵ���ת��Ũ�ȱ���ʼŨ�ȡ�
(3)�����ƽ����Է������� ��仯��m����n�����йء�
��仯��m����n�����йء�
��(1)ʹƽ��ʱc(CO)/c(CO2)��������Ҫʹƽ��������Ӧ�����ƶ���CO2��Ũ�ȼ�С��CO��Ũ������ ��ֵ����ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ������У�A�ԣ���Ӧǰ����������ʵ������䣬����ѹǿƽ�ⲻ�ƶ���B��������N2��ƽ��û��Ӱ�죬C�������۵����Ķ��ٶ�ƽ��û��Ӱ�죬D����
(2)����CO2��Ũ�ȣ���Ӧ����ֻ��CO2Ϊ���壬�ҷ�Ӧǰ�����������ȡ��൱������ѹǿ��ƽ�ⲻ�����ƶ���CO2��ת���ʲ��䡣
��(1)��Ϊ�ں�ѹ�����н��У�ѹǿһֱ���䣬A������v��(CO)=v��(H2O)ʱ����Ӧ�ﵽƽ�⣬B�ԣ��κ�ʱ�����ɵ�CO��H2���ʵ�������ȣ�C����1 mol H��H������˵����1 mol H2��Ӧ������2 mol H��O��˵����1 mol H2O��Ӧ����Ӧ�ﵽƽ�⣬D�ԡ�
(2)ԭƽ��״̬��CO��H2��ƽ����Է�������Ϊ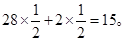 ��ѹʱƽ�������ƶ���H2O(g)(��Է�������Ϊ18)�ĺ�������������ƽ����Է�����������
��ѹʱƽ�������ƶ���H2O(g)(��Է�������Ϊ18)�ĺ�������������ƽ����Է�����������
(1)����CO��CO2��Ũ�ȱ�ֵ��ϵ�ó�ƽ���ƶ��ķ���Ȼ���ٽ����жϡ�
(2)����Ӧ���Ũ�ȣ���Ӧ���ת���ʲ�һ����С��ת���ʵ���ת��Ũ�ȱ���ʼŨ�ȡ�
(3)�����ƽ����Է�������
 ��仯��m����n�����йء�
��仯��m����n�����йء���(1)ʹƽ��ʱc(CO)/c(CO2)��������Ҫʹƽ��������Ӧ�����ƶ���CO2��Ũ�ȼ�С��CO��Ũ������ ��ֵ����ӦΪ���ȷ�Ӧ�������¶�ƽ��������Ӧ������У�A�ԣ���Ӧǰ����������ʵ������䣬����ѹǿƽ�ⲻ�ƶ���B��������N2��ƽ��û��Ӱ�죬C�������۵����Ķ��ٶ�ƽ��û��Ӱ�죬D����
(2)����CO2��Ũ�ȣ���Ӧ����ֻ��CO2Ϊ���壬�ҷ�Ӧǰ�����������ȡ��൱������ѹǿ��ƽ�ⲻ�����ƶ���CO2��ת���ʲ��䡣
��(1)��Ϊ�ں�ѹ�����н��У�ѹǿһֱ���䣬A������v��(CO)=v��(H2O)ʱ����Ӧ�ﵽƽ�⣬B�ԣ��κ�ʱ�����ɵ�CO��H2���ʵ�������ȣ�C����1 mol H��H������˵����1 mol H2��Ӧ������2 mol H��O��˵����1 mol H2O��Ӧ����Ӧ�ﵽƽ�⣬D�ԡ�
(2)ԭƽ��״̬��CO��H2��ƽ����Է�������Ϊ
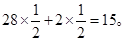 ��ѹʱƽ�������ƶ���H2O(g)(��Է�������Ϊ18)�ĺ�������������ƽ����Է�����������
��ѹʱƽ�������ƶ���H2O(g)(��Է�������Ϊ18)�ĺ�������������ƽ����Է�����������
��ϰ��ϵ�д�
 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
�����Ŀ
 ��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��??
��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��??
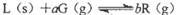 �ﵽƽ��ʱ���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ��ͼ��ѹǿP1>P2��x���ʾ�¶ȣ�y���ʾƽ��������G������������ݴ˿��ж�( )��
�ﵽƽ��ʱ���¶Ⱥ�ѹǿ�Ը÷�Ӧ��Ӱ����ͼ��ʾ��ͼ��ѹǿP1>P2��x���ʾ�¶ȣ�y���ʾƽ��������G������������ݴ˿��ж�( )��
 C(g)��D(g) ��H��0����ش���������:
C(g)��D(g) ��H��0����ش���������: WI2(g) (I)���÷�Ӧ��ʯӢ��չ��н��У�����ͼ��ʾ��
WI2(g) (I)���÷�Ӧ��ʯӢ��չ��н��У�����ͼ��ʾ��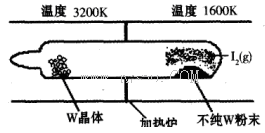
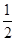 ����ij�����ܱ������м���1mol I2(g)������W(s)����Ӧ�ﵽƽ��ʱI2(g)��ת����Ϊ__________��
����ij�����ܱ������м���1mol I2(g)������W(s)����Ӧ�ﵽƽ��ʱI2(g)��ת����Ϊ__________��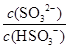 ��________�����������С�����䡱����
��________�����������С�����䡱���� CO2(g)+H2(g) ��H<0��
CO2(g)+H2(g) ��H<0��