题目内容
某恒温密闭容器中,可逆反应A(s)??B+C(g) ΔH=Q kJ/mol (Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是( )
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q
AB
若B是气体,平衡常数K=c(B)·c(C),若B是非气体,平衡常数K=c(C),由于C(g)的浓度不变,因此B是非气体,A正确,C错误,根据平衡的v(正)=v(逆)可知B正确(注意,不是浓度消耗相等);由于反应是可逆反应,因此达到平衡时放出热量小于Q,D项错误。

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
 N2O4(g),此时平衡混合气中NO2的体积分数为X%,若再充入1 mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为Y%,则X和Y的大小关系正确的是 ( )
N2O4(g),此时平衡混合气中NO2的体积分数为X%,若再充入1 mol N2O4,在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为Y%,则X和Y的大小关系正确的是 ( ) B(g)+3C(g),下列四项中处于平衡状态的是( )
B(g)+3C(g),下列四项中处于平衡状态的是( ) 2CO(g) ΔH>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。
2CO(g) ΔH>0,测得容器中CO2的物质的量随时间t的变化关系如图所示。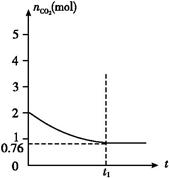
 Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) 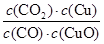
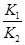
 CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
CH3OH(g)+H2O(g) ΔH<0,容器中CH3OH的物质的量随时间变化如曲线Ⅰ所示,平衡时容器内压强为p1。改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
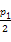
 FeO(s)+CO(g) ΔH>0。
FeO(s)+CO(g) ΔH>0。 CO(g)+H2(g),试分析和回答下列问题:
CO(g)+H2(g),试分析和回答下列问题: 2HF
2HF
 2Z(g)
2Z(g)