题目内容
CO、H2在一定条件下合成乙醇:2CO(g)+4H2(g)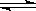 CH3CH2OH(g)+H2O(g) △H=—255.6 kJ·mol—1,下列说法错误的是
CH3CH2OH(g)+H2O(g) △H=—255.6 kJ·mol—1,下列说法错误的是
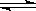 CH3CH2OH(g)+H2O(g) △H=—255.6 kJ·mol—1,下列说法错误的是
CH3CH2OH(g)+H2O(g) △H=—255.6 kJ·mol—1,下列说法错误的是| A.反应物的总能量大于生成物的总能量 |
| B.增大H2浓度可以使CO转化率达到100℅ |
| C.使用合适的催化剂、升高温度均可加大反应速率 |
| D.反应达到平衡时,正反应和逆反应的化学反应速率相等且不为零 |
B
根据热化学方程式可知,反应是放热反应,所以反应物的总能量高于生成物的总能量,A正确;可逆反应的转化率不可能达到100%,B不正确;催化剂能降低反应的活化能,增大反应速率,C正确;在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项D正确,答案选B。

练习册系列答案
相关题目
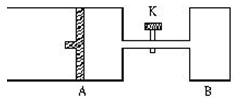
 2Z+2W+Q;ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2aL。试回答:
2Z+2W+Q;ΔH<0(X、Y、Z、W均为气体),达到平衡时,VA=1.2aL。试回答: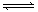 2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据右图回答:从t2→t3的曲线变化是由哪种条件引起的( )
2Z(g) △H<0。从反应开始经过t1后达到平衡状态,t2时由于条件改变,平衡受到破坏,在t3时又达到平衡,据右图回答:从t2→t3的曲线变化是由哪种条件引起的( )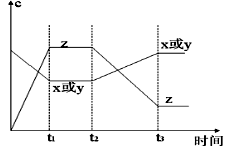
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
 ?pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )
?pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是( )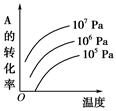
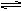 2Z(g), 若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1 mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是( )
2Z(g), 若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1 mol·L-1,0.3 mol·L-1,0.08 mol·L-1,则下列判断不合理的是( )  N2O4△H<0,则以下说法正确的是
N2O4△H<0,则以下说法正确的是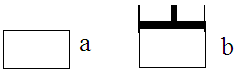
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则: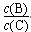 将________。
将________。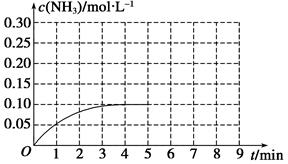
 C(g)+D(g),5min后达平衡,各物质的平衡浓度的关系为[c(A)]a·c(B)= c(C)·c(D)。若在温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为
C(g)+D(g),5min后达平衡,各物质的平衡浓度的关系为[c(A)]a·c(B)= c(C)·c(D)。若在温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为