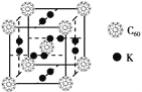
��Ŀ����
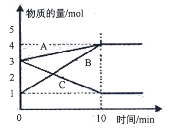
����Ŀ��ij�¶�����2L�ܱ������У�3����̬����A��B��C�����ʵ�����ʱ��仯������ͼ��
��1���÷�Ӧ�Ļ�ѧ����ʽ��________________________
��2����A��B��C��Ϊ���壬10min��Ӧ�ﵽƽ�⣬
�ٴ�ʱ��ϵ��ѹǿ�ǿ�ʼʱ��________����
���ڸ������ﵽƽ��ʱ��Ӧ���ת����Ϊ________%������������1λС����
��3�����ڸ÷�Ӧ��˵����ȷ����_________��
a.����10minʱֹͣ��Ӧ
b.�ڵ���10min֮ǰC������������ʴ���������������
c.��10minʱB���������Ӧ���ʵ����淴Ӧ����
���𰸡�2C![]() A+3B
A+3B ![]() ��1.29��1.3 66.7% b��c
��1.29��1.3 66.7% b��c
��������
��1����ͼ��֪��C�Ƿ�Ӧ����ʵ����ֱ����2mol��A��B��������ʵ�������1mol��3mol�����ʵ����仯�ȵ���ϵ���ȣ�
��2������ϵ��ѹǿ�ȵ������ʵ����ȣ�
��ת����=�仯������ʼ����100%��
��3�����ݻ�ѧƽ��Ķ����жϣ�
��1����ͼ��֪��C�Ƿ�Ӧ����ʵ�������2mol��A��B��������ʵ����ֱ�����1mol��3mol�����ʵ����仯�ȵ���ϵ���ȣ����Ը÷�Ӧ�Ļ�ѧ����ʽΪ��2C![]() A+3B��
A+3B��
��2������ϵ��ѹǿ�ȵ������ʵ����ȣ���Ӧǰ���������ʵ�����7mol����Ӧ�����������ʵ�����9mol�����Դ�ʱ��ϵ��ѹǿ�ǿ�ʼʱ��![]() ����
����
��ת����=�仯������ʼ����100%=2��3��100%=66.7%��
��3��a.����ͼ����10minʱ��Ӧ�ﵽƽ��״̬�����淴Ӧ������ȵ���Ϊ0����Ӧû��ֹͣ����a����
b.�ڵ���10min֮ǰ��C�����ʵ������٣����� C������������ʴ��������������ʣ���b��ȷ��
c.��10minʱ��Ӧ�ﵽƽ��״̬������B���������Ӧ���ʵ����淴Ӧ���ʣ���c��ȷ��
ѡbc��

����Ŀ���Թ�ҵ������ɰ���÷�����þ��Ϊԭ����ȡMgSO4��7H2O�Ĺ�����ͼ��ʾ��

��þ�����Ҫ�ɷ����±���
MgO | SiO2 | FeO��Fe2O3 | CaO | Al2O3 | B2O3 |
30%~40% | 20%~25% | 5%~15% | 2%~3% | 1%~2% | 1%~2% |
�ش��������⣺
��1������⡱ʱӦ�ü��������_______��������1������Ҫ����_________��д��ѧʽ����
��2�������ӡ�ʱ���������ơ�����þ�����÷ֱ���________��_______��
��3���жϡ����ӡ�������ɵļ��鷽����____________��
��4����������3Ӧ���ȹ��˵�ԭ����___________��
����Ŀ����16�֣���ҵ�Ͽ����ں����ܱ������в������з�Ӧ�Ʊ��״���
CO��g����2H2��g��![]() CH3OH��g��
CH3OH��g��
��1���������������Ϊ�жϷ�Ӧ�ﵽƽ��״̬�����ݵ��ǣ�����ţ� ��
A������CH3OH ������������H2������֮��Ϊ1�U2
B����������ƽ����Է����������ֲ���
C�����������ܶȱ��ֲ���
D����ϵ�ڵ�ѹǿ���ֲ���
��2���±���������Ϊ�÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����
�¶�/�� | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
����Ӧ��ƽ�ⳣ������ʽΪK= �����ϱ������жϣ��÷�Ӧ����H 0�����������������������������������¶ȣ�����Ӧ���� ������������������С����������������
��ij�¶��£���2molCO��6molH2����һ���ݻ�Ϊ2L���ܱ������У��ﵽƽ��ʱc(H2)=1.4mol/L����CO��ת����Ϊ ����ʱ���¶�Ϊ ��
��3�������CO��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��������ţ�
A������
B���������Ч�Ĵ���
C�����������³���CO
D�����������³���H��
E�����������³��뺤��
F����ʱ����CH3OH
��4��һ�������£�CO��H2�ڴ�������������1molCH3OH�������仯Ϊ90.8kJ�����¶��£��������ݻ���ͬ���ܱ������У�����ͬ��ʽͶ�ϣ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й��������£�
���� | �� | �� | �� | |
Ͷ�Ϸ�ʽ | 1molCO��2molH2 | 1molCH3OH | 2molCH3OH | |
ƽ������ | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
��ϵѹǿ(Pa) | p1 | p2 | p3 | |
��Ӧ�������仯 | akJ | bkJ | ckJ | |
ԭ��ת���� | ��1 | ��2 | ��3 | |
���з�����ȷ���� ��������ţ�
A��2c1��c3 B��2 p1��p3C��|a|��|b|��90.8 D����1����3��1
����Ŀ���±���ʵ���������������۶�Ӧ��ϵ��ȷ����
ѡ�� | ʵ����� | ʵ������ | ���� |
A | �Է�̪Ϊָʾ�����������Һ�ζ�����������Һ | ��Һ�ɺ�ɫ��Ϊdz��ɫ�����̶��� | �������������Һ��Ũ��ƫ�� |
B | ���з�̪��Na2CO3��Һ�м�������BaC12���� | �а�ɫ�������ɣ���Һ��ɫ��dz | ֤��������Һ�ʼ�������CO32-ˮ������� |
C | �����·ֱ�ⶨNaClO��Һ��CH3COONa��Һ��pH | ǰ�ߴ� | ���ԣ�HClO>CH3COOH |
D | NaHCO3��Һ�е����̪ | ��Һ��� | �������ʽ����Һ���ʼ��� |
A. A B. B C. C D. D