题目内容
【题目】以![]() 、软锰矿(主要成分为
、软锰矿(主要成分为![]() ,少量
,少量![]() 及
及![]() 的化合物等)、氨水及净化剂等为原料可制备
的化合物等)、氨水及净化剂等为原料可制备![]() 液和
液和![]() ,主要实验步骤如下
,主要实验步骤如下

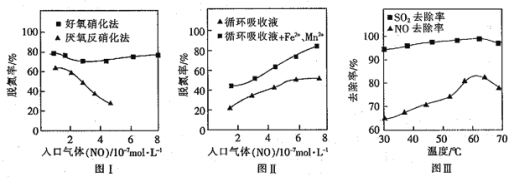
步骤I、如图所示装置,将![]() 通入
通入![]() 中的软锰矿浆液中
中的软锰矿浆液中![]() 。
。
步骤II、充分反应后,在不断搅拌下依次向仪器![]() 中加入适量纯净的
中加入适量纯净的![]() ,最后加入适量
,最后加入适量![]() 沉铅,
沉铅,
步骤III、过滤得![]() 溶液
溶液
(1)仪器R的名称是_______。
(2)装置![]() 用于制取
用于制取![]() ,反应的化学方程式为_________。
,反应的化学方程式为_________。
(3)装置![]() 中的反应应控制在90~100℃,适宜的加热方式是______________。
中的反应应控制在90~100℃,适宜的加热方式是______________。
(4)装置![]() 的作用是______________________。
的作用是______________________。
(5)“步骤Ⅱ”中加入纯净![]() 的目的是_______________,用
的目的是_______________,用![]() 调节溶液
调节溶液![]() 时,需调节溶液
时,需调节溶液![]() 的范围为________(该实验条件下,部分金属离子开始沉淀和沉淀完全的
的范围为________(该实验条件下,部分金属离子开始沉淀和沉淀完全的![]() 如下表)
如下表)
金属离子 |
|
|
|
|
开始沉淀的 | 7.04 | 1.87 | 3.32 | 7.56 |
沉淀完全的 | 9.18 | 3.27 | 4.9 | 10.2 |
(6)已知①用空气氧化![]() 浊液可制备
浊液可制备![]() ,主要副产物为
,主要副产物为![]() ;反应温度和溶液
;反应温度和溶液![]() 对产品中
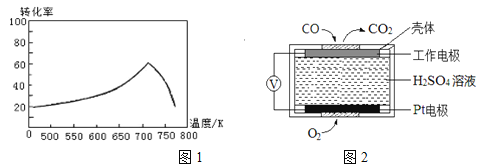
对产品中![]() 的质量分数的影响分别如图所示
的质量分数的影响分别如图所示

②反应温度超过![]() 时,
时,![]() 的产率开始降低,
的产率开始降低,![]() 是白色沉淀,
是白色沉淀,![]() 呈黑色;
呈黑色;![]() 、
、![]() 中锰的质量分数理论值依次为72.05%、62.5%请补充完整由步骤III得到
中锰的质量分数理论值依次为72.05%、62.5%请补充完整由步骤III得到![]() 溶液,并用氨水等制备较纯净的
溶液,并用氨水等制备较纯净的![]() 的实验方案:______________________,真空干燥6小时得产品
的实验方案:______________________,真空干燥6小时得产品![]() 。
。
【答案】三颈烧瓶 ![]() 用
用![]() 的水浴加热 吸收未反应的
的水浴加热 吸收未反应的![]() ,防止污染环境 将
,防止污染环境 将![]() 氧化为
氧化为![]()
![]() 将滤液加热并保温在
将滤液加热并保温在![]() ,用氨水调节溶液
,用氨水调节溶液![]() 并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出
并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出![]()
【解析】
由装置图结合实验步骤可知,以![]() 、软锰矿(主要成分为
、软锰矿(主要成分为![]() ,少量
,少量![]() 及
及![]() 的化合物等)、氨水及净化剂等为原料可制备
的化合物等)、氨水及净化剂等为原料可制备![]() 液和
液和![]() ,装置A制取SO2,装置B通入SO2与MnO2反应得到MnSO4,在不断搅拌下向仪器R中加入适量纯净的MnO2,将
,装置A制取SO2,装置B通入SO2与MnO2反应得到MnSO4,在不断搅拌下向仪器R中加入适量纯净的MnO2,将![]() 氧化为
氧化为![]() ,再加入MnCO3调节溶液pH,使Fe3+和Al3+形成沉淀而除去;最后加入适量
,再加入MnCO3调节溶液pH,使Fe3+和Al3+形成沉淀而除去;最后加入适量![]() 沉铅,过滤得
沉铅,过滤得![]() 溶液;装置C中盛有NaOH溶液,用来吸收未反应的
溶液;装置C中盛有NaOH溶液,用来吸收未反应的![]() ,防止污染环境。
,防止污染环境。
滤液中含有MnSO4,控制温度在![]() ,调节溶液
,调节溶液![]() 并维持8~9。用空气氧化生成的Mn(OH)2得到黑色沉淀Mn3O4,过滤,洗涤、干燥得产品
并维持8~9。用空气氧化生成的Mn(OH)2得到黑色沉淀Mn3O4,过滤,洗涤、干燥得产品![]() 。据此解答。
。据此解答。
(1)由仪器构造可知仪R的名称是三颈烧瓶,
故答案为:三颈烧瓶;
(2)装置![]() 中亚硫酸钠固体和硫酸反应生成硫酸钠、水和
中亚硫酸钠固体和硫酸反应生成硫酸钠、水和![]() ,化学方程式为
,化学方程式为![]() ,
,
故答案为:![]() ;
;
(3)由于需要控制温度在90~100℃,所以适宜的加热方式是用![]() 的水浴加热,
的水浴加热,
故答案为:用![]() 的水浴加热;
的水浴加热;
(4) 装置C中盛有NaOH溶液,用来吸收未反应的![]() ,防止污染环境,
,防止污染环境,
故答案为:吸收未反应的![]() ,防止污染环境;
,防止污染环境;
(5)除杂过程中加入纯净![]() 的目的是将
的目的是将![]() 氧化为
氧化为![]() ;用
;用![]() 调节溶液
调节溶液![]() 时,使Fe3+、Al3+沉淀完全,而Mn2+不沉淀,需调节溶液
时,使Fe3+、Al3+沉淀完全,而Mn2+不沉淀,需调节溶液![]() 的范围为
的范围为![]() ,
,
故答案为:将![]() 氧化为
氧化为![]() ;
;![]() ;
;
(6)由图象可知,应选择的反应条件是:温度![]() ,溶液pH为8~9;实验方案设计为:将滤液加热并保温在
,溶液pH为8~9;实验方案设计为:将滤液加热并保温在![]() ,用氨水调节溶液
,用氨水调节溶液![]() 并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出
并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出![]() ,
,
故答案为:将滤液加热并保温在![]() ,用氨水调节溶液
,用氨水调节溶液![]() 并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出
并维持8~9。在不断搅拌下,边通空气边滴加氨水,直至有大量黑色沉淀,静置,在上层清液中再滴加氨水至无沉淀。过滤,洗涤沉淀直至过滤液中检测不出![]() 。
。

 备战中考寒假系列答案
备战中考寒假系列答案【题目】工业上,常用O2氧化HCl转化成Cl2,提高效益,减少污染。反应为:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
2Cl2(g)+2H2O(g)。一定条件下,测得数据如下:
t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 | 10.0 |
c(Cl2)/10-3molL-1 | 0 | 1.8 | 3.7 | 5.4 | 7.2 | 7.2 |
下列说法错误的是( )
A.条件不变时,12min时v正(Cl2)=v逆(H2O)
B.2.0~4.0min内的平均反应速率大于6.0~8.0min内的
C.0~8.0min内HCl的平均反应速率为1.8mol·L-1·min-1
D.加入高效催化剂,达到平衡所用时间小于8.0min