题目内容
4.通过量CO2于下列溶液中,出现浑浊的是( )| A. | Ba(NO3)2溶液 | B. | 饱和澄清石灰水 | C. | Na2SO4溶液 | D. | 饱和Na2CO3溶液 |
分析 A、碳酸不能与强酸盐Ba(NO3)2反应生成强酸和弱酸盐;
B、当CO2过量时生成碳酸氢钙;
C、碳酸不能与强酸盐Na2SO4反应生成强酸和弱酸盐;
D、碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3.
解答 解:A、因酸与盐反应一般规律是:强酸与弱酸盐反应生成弱酸和强酸的盐,像本选项中碳酸不能与强酸盐Ba(NO3)2反应生成强酸和弱酸盐,所以自始至终也不出现浑浊,故A错误;
B、石灰水与CO2反应生成碳酸钙沉淀,当CO2过量时,碳酸钙又与二氧化碳和水继续反应生成碳酸氢钙而使沉淀消失.故B错误;
C、因酸与盐反应一般规律是:强酸与弱酸盐反应生成弱酸和强酸的盐,由于碳酸的酸性小于H2SO4 的酸性,所以碳酸不能与Na2SO4反应,故C错误;
D、因碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3,故最终有碳酸氢钠析出而使溶液变浑浊,故D正确;
故选:D.
点评 本题考查了CO2的相关性质,酸与盐反应一般规律是:强酸与弱酸盐反应生成弱酸和强酸的盐.但要注意在酸与盐反应的问题上有些特例,如CuSO4+H2S═CuS↓+H2SO4.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
14.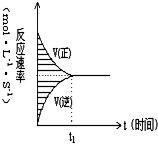 在容积固定的4L密闭容器中,进行可逆反应X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率υ(正)、υ(逆)与时间t的关系如右图,如图中阴影部分面积表示( )
在容积固定的4L密闭容器中,进行可逆反应X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率υ(正)、υ(逆)与时间t的关系如右图,如图中阴影部分面积表示( )
 在容积固定的4L密闭容器中,进行可逆反应X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率υ(正)、υ(逆)与时间t的关系如右图,如图中阴影部分面积表示( )
在容积固定的4L密闭容器中,进行可逆反应X(g)+2Y(g)?2Z(g)并达到平衡,在此过程中,以Y的浓度改变表示的反应速率υ(正)、υ(逆)与时间t的关系如右图,如图中阴影部分面积表示( )| A. | X的浓度的减少 | B. | Y的物质的量的减少 | ||
| C. | Y的浓度的减少 | D. | X的物质的量的减少 |
15.下列判断中正确的是( )
| A. | 可用澄清石灰水来区分二氧化碳和二氧化硫 | |
| B. | 可用无水硫酸铜检验酒精中是否含少量水 | |
| C. | 能使灼热的CuO由黑变红的气体一定是H2 | |
| D. | 可用石蕊试液来鉴别盐酸和醋酸 |
12.下列说法中,不正确的是( )
| A. | SiO2是酸性氧化物,但不与水反应 | |
| B. | 泡花碱属于盐类 | |
| C. | 明矾和漂白粉均可用于自来水的杀菌、消毒 | |
| D. | 玻璃和陶瓷都属于传统硅酸盐材料 |
19.下列叙述中正确的是( )
| A. | H2SO4的摩尔质量是98 | |
| B. | 2mol NO中含2mol氮和2mol O | |
| C. | 等质量的O2和O3中所含氧原子个数相同 | |
| D. | 1mol O22-的质量为34g |
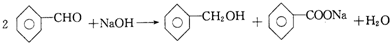
5. 苯甲醛在浓碱的条件下能发生歧化反应生成苯甲醇和苯甲酸盐.某实验小组利用该原理制备纯净的苯甲酸.
苯甲醛在浓碱的条件下能发生歧化反应生成苯甲醇和苯甲酸盐.某实验小组利用该原理制备纯净的苯甲酸.
查阅相关文献,可能用到的有关数据如下:
表1:有关物质的密度、沸点、溶解性
表2:苯甲酸为白色片状晶体,熔点122.4℃,苯甲酸在水中的溶解度见下表
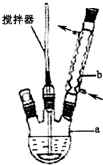
实验方法:在图示反应装置中,加入反应物搅拌下控温55℃回流至瓶内物质成糊状后完成.拆除装置,往仪器a中加入适量水,搅拌使固体溶解,然后将反应混合物转入分液漏斗中,用30ml萃取剂分3次萃取.往萃取后的水层中加入30g碎冰,在搅拌下慢慢加入浓HCl至湿润的紫色石蕊试纸变红,冰水浴中冷却析出苯甲酸粗品.请回答下列问题:
(1)写出装置图中玻璃仪器的名称,a三颈烧瓶,b(球形)冷凝管.
(2)为了进一步提纯苯甲酸,通常采用重结晶法进行.在进行该实验过程中需要趁热过滤.将粗笨甲酸全溶后往往需要再加入少量蒸馏水的目的是为了减少趁热过滤过程中损失苯甲酸.
(3)将提炖后的产品进行洗涤、干燥.检验经上述操作后得到的是否是纯净的苯甲酸的常用方法是测定获得产品的熔点是否是122.4℃.
(4)在整个过程中,若苯甲醛所取的质量为2.120g,最终获取的纯净笨甲酸的质量为1.098g,则苯甲酸的产率为90.0%.
(5)某同学认为可从弃去的萃取有机层中获取笨甲醇,为完成该实验需要的玻璃仪器有温度计、尾接管及蒸馏烧瓶、直形冷凝管、锥形瓶.
 苯甲醛在浓碱的条件下能发生歧化反应生成苯甲醇和苯甲酸盐.某实验小组利用该原理制备纯净的苯甲酸.
苯甲醛在浓碱的条件下能发生歧化反应生成苯甲醇和苯甲酸盐.某实验小组利用该原理制备纯净的苯甲酸.
查阅相关文献,可能用到的有关数据如下:
表1:有关物质的密度、沸点、溶解性
| 物质 | 相对分子 质量 | 密度/ (相对于水) | 沸点/℃ | 溶解性 |
| 苯甲醛 | 106 | 1.046 | 178.8 | 微溶于水,可混溶于乙醇、乙醚、苯、氯仿 |
| 苯甲醇 | 108 | 1.042 | 205.7 | 溶于水,易溶于乙醇、醚、芳烃 |
| 苯甲酸 | 122 | 1.271 | 249.2 | 微溶于水,易溶于乙醇、乙醚、氯仿、苯、二硫化碳、四氯化碳 |
| 苯甲酸钠 | 144 | 1.442 | 249.3 | 溶于水和乙醇、甘油、苯、甲醇、微溶于乙醚 |
| 温度/℃ | 25 | 50 | 95 |
| 溶解度/g | 0.17 | 0.95 | 6.8 |
(1)写出装置图中玻璃仪器的名称,a三颈烧瓶,b(球形)冷凝管.
(2)为了进一步提纯苯甲酸,通常采用重结晶法进行.在进行该实验过程中需要趁热过滤.将粗笨甲酸全溶后往往需要再加入少量蒸馏水的目的是为了减少趁热过滤过程中损失苯甲酸.
(3)将提炖后的产品进行洗涤、干燥.检验经上述操作后得到的是否是纯净的苯甲酸的常用方法是测定获得产品的熔点是否是122.4℃.
(4)在整个过程中,若苯甲醛所取的质量为2.120g,最终获取的纯净笨甲酸的质量为1.098g,则苯甲酸的产率为90.0%.
(5)某同学认为可从弃去的萃取有机层中获取笨甲醇,为完成该实验需要的玻璃仪器有温度计、尾接管及蒸馏烧瓶、直形冷凝管、锥形瓶.
3. 某化学兴趣小组根据反应:Mg+H2SO4═MgSO4+H2↑设计测定镁原子摩尔质量的实验,实验的简易装置如图,除去表面氧化膜的镁条的质量为0.24g.镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积),下列关于该实猃的叙述不正确的是( )
某化学兴趣小组根据反应:Mg+H2SO4═MgSO4+H2↑设计测定镁原子摩尔质量的实验,实验的简易装置如图,除去表面氧化膜的镁条的质量为0.24g.镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积),下列关于该实猃的叙述不正确的是( )
 某化学兴趣小组根据反应:Mg+H2SO4═MgSO4+H2↑设计测定镁原子摩尔质量的实验,实验的简易装置如图,除去表面氧化膜的镁条的质量为0.24g.镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积),下列关于该实猃的叙述不正确的是( )
某化学兴趣小组根据反应:Mg+H2SO4═MgSO4+H2↑设计测定镁原子摩尔质量的实验,实验的简易装置如图,除去表面氧化膜的镁条的质量为0.24g.镁条完全反应后,用量筒收集水,体积为0.224L(设已折换成标准状况下的对应的气体体积),下列关于该实猃的叙述不正确的是( )| A. | 实验前应检验装置的气密性 | |
| B. | 装置乙中的水不可以用NaCl溶液代替 | |
| C. | 读数时,应使装置乙和装置丙中的液面处于同一水平面上 | |
| D. | 镁原子的摩尔质量为24.0 g.mol-1 |

 A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示: