题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.使pH试纸变蓝的溶液中:![]() 、Na+、Cl-、ClO-
、Na+、Cl-、ClO-
B.1.0 mol·L-1的HNO3溶液中:K+、[Ag(NH3)2]+、Cl-、![]()
C.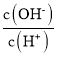 =1的溶液中:Fe2+、
=1的溶液中:Fe2+、![]() 、Al3+、I-
、Al3+、I-
D.0.1 mol·L-1的NH4HCO3溶液中:K+、Na+、![]() 、Cl-
、Cl-
【答案】D
【解析】
A.使pH试纸变蓝的溶液呈碱性,溶液中存在大量氢氧根离子,![]() 与氢氧根离子反应,在溶液中不能大量共存,故A不符合题意;
与氢氧根离子反应,在溶液中不能大量共存,故A不符合题意;
B.1.0 mol·L-1的HNO3溶液酸性较强,[Ag(NH3)2]+不能稳定存在,会产生银离子,银离子和氯离子会生成不溶于硝酸的沉淀,故B不符合题意;
C.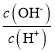 =1的溶液显中性,Fe2+、Al3+、
=1的溶液显中性,Fe2+、Al3+、![]() 均不能在中性溶液中大量存在,且Fe2+、Al3+和
均不能在中性溶液中大量存在,且Fe2+、Al3+和![]() 会发生双水解,故C不符合题意;
会发生双水解,故C不符合题意;
D.四种离子之间相互不反应,也不与碳酸氢铵反应,可以大量共存,故D符合题意;
故答案为D。

练习册系列答案
相关题目