题目内容
【题目】白铁皮在发生析氢腐蚀时有0.2mol电子转移,下列说法正确的是( )
A.有5.6 g金属被腐蚀
B.有6.5 g金属被氧化
C.有0.15 mol金属失去电子
D.标准状况下有4.48 L H2逸出
【答案】B
【解析】解:镀锌铁在发生析氢腐蚀时,较活泼的金属锌作负极,较不活泼的金属铁作正极,负极上锌失电子而被腐蚀,正极上氢离子得电子被还原.
根据Zn﹣2e﹣=Zn2+得,腐蚀锌的质量= ![]() ×65g/mol=6.5g,故有6.5 g金属被氧化,根据2H++2e﹣=H2 ↑得,生成氢气的体积=
×65g/mol=6.5g,故有6.5 g金属被氧化,根据2H++2e﹣=H2 ↑得,生成氢气的体积= ![]() ×22.4L/mol=2.24L.
×22.4L/mol=2.24L.
故选B.
白铁皮即镀锌铁在发生析氢腐蚀时,较活泼的金属锌作负极,较不活泼的金属铁作正极,负极上锌失电子而被腐蚀,正极上氢离子得电子被还原,根据金属、氢气和转移电子之间的关系式计算.

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题: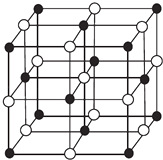
(1)写出C、D、E三种原子第一电离能由大到小的顺序为 . (用元素符号表示)
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为(用分子式表示),根据价层电子对互斥理论预测BA2D的分子构型为 .
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据六面体互不相邻的顶点,而六面体的每条棱上均有一个BC﹣ . 与A同族且相隔两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示) .
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
离子晶体 | NaCl | KCl | CaO |
晶格能/kJmol﹣1 | 786 | 715 | 3401 |
根据表格中的数据:判断KCl、MgO、TiN三种离子晶体熔点从高到低的顺序是 . MgO晶体中一个Mg2+周围和它最邻近且等距离的O2﹣有个.
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是 .