题目内容
【题目】Na2CO3、NaHCO3是生活在常见的盐,某实验小组通过以下实验了探究这两种物质的性质(已知:Na2CO3、NaHCO3的水溶液均呈碱性;NaHCO3受热易分解生成Na2CO3、H2O和CO2)。
(1)称取两种固体各1g分别放入两支试管中,在各加入5mL水,振荡。固体成分溶解,并恢复至室温。
①发现Na2CO3完全溶解,而NaHCO3有剩余。由此得出结论:在相同温度下,________。
②向所得溶液中各滴入1~2滴酚酞溶液后,溶液均显________色。
(2)①取少量NaHCO3按下图装置进行实验。可观察到的现象是:大试管口有水珠生成,________________。
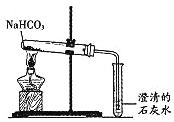
②用______________的方法除去混在Na2CO3粉末中少量的NaHCO3。
(3)测定Na2CO3样品(含氯化钠杂质)中Na2CO3的质量分数:
①称取mg样品放入烧杯内加水溶解。
②加入过量的氯化钙溶液充分反应,反应的化学方程式为_________________;证明反应后氯化钙有剩余的方法是______________________________。
③过滤、洗涤、干燥,称量沉淀的质量为ng。则样品中Na2CO3的质量分数为______。
【答案】碳酸钠的溶解度比碳酸氢钠的大红色澄清的石灰水变浑浊加热CaCl2+Na2CO3=CaCO3↓+2NaCl向反应后所得溶液中加入碳酸钠,有沉淀生成![]()
【解析】
(1)①称取两种固体各1g,分别放入两个小烧杯中,再各滴加5mL蒸馏水,振荡,测量温度变化;待固体充分溶解,并恢复至室温后,发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,说明在同样的温度下,同质量的两种固体在同体积的溶剂中,Na2CO3比NaHCO3易溶于水,即碳酸钠的溶解度比碳酸氢钠的大;
②碳酸钠和碳酸氢钠的溶液显碱性,向所得溶液中各滴入1~2滴酚酞溶液后,溶液均呈红色;
(2)①碳酸氢钠受热易分解:2NaHCO3![]() Na2CO3+CO2↑+H2O,因此可观察带的现象是:大试管口有水珠生成,生成的CO2气体通入澄清石灰水,澄清石灰水变浑浊;
Na2CO3+CO2↑+H2O,因此可观察带的现象是:大试管口有水珠生成,生成的CO2气体通入澄清石灰水,澄清石灰水变浑浊;
②碳酸钠加热不分解,碳酸氢钠受热易分解,因此用加热的方法可除去混在Na2CO3粉末中的少量的NaHCO3;
(3)②碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,化学方程方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl,证明反应后CaCl2有剩余的方法是再加入碳酸钠,有白色沉淀生成;
③设碳酸钠样品中碳酸钠的质量为xg,则根据方程式可知
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x n
106:x=100:n
解得x=106n/100
因此样品中Na2CO3的质量分数为![]() 。
。

【题目】能源是人类生存与发展必不可缺的物质,对传统能源进行脱硫、脱硝处理,能提高能源在能源消费中的比例是改变目前我国频发的雾霾天气的有效措施。
(1)肼(N2H4)和化合物甲是一种重要的火箭推进剂,甲分子与肼分子具有相同的电子数,二者反应的生成物中有10e-分子,另一种生成物为极稳定的单质,写出该反应的化学方程式__________________。
(2)对燃煤产生的尾气进行回收处理,有助于空气质量的改善,还能变废为宝,尾气处理过程中涉及到的主要反应如下:
①2CO(g)+SO2(g)=S(g)+2CO2(g) △H=十8.0 kJ·mol-1
②2H2 (g)+SO2(g)=S(g)+2H2O(g) △H=+90.4 kJ·mol-1
③2CO(g)+O2 (g) =2CO2 (g) △H= -566.0 kJ·mol-1
④2H2 (g)+O2 (g) =2H2O(g) △H =-483.6 kJ·mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式为__________________。
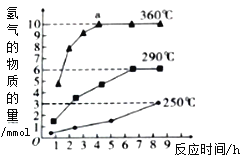
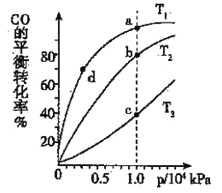
(3)煤炭液化也有助于减少雾霾天气的发生,液化反应之一为:CO(g)+2H2(g)![]() CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为__________;实际生产条件控制在T 1°C、1×106Pa左右,选择此压强的理由是________。
CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为__________;实际生产条件控制在T 1°C、1×106Pa左右,选择此压强的理由是________。
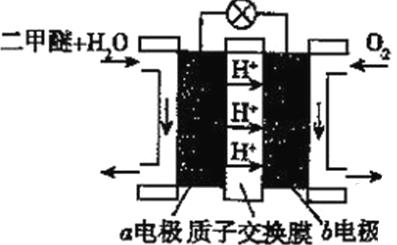
(4)工业上生产新能源二甲醚(CH3OCH3)的原理之一为:2CO(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:
CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:
容器 | c(CO) | c(H2) | c(CH3OCH3) | c(H2O) | v(正)与v(逆)大小比较 |
I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v(正)= v(逆) |
II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 | v(正)____v(逆)(填“>” |
填写表中空白处,并写出其推测过程___________。
(5)二甲醚(燃烧热为1455kJ/mol)燃料电池是一种绿色电池,其工作原理如图所示,a、b均为惰性电极,a极的电极反应式为________________________;当消耗1molO2时,通过质子交换膜的质子数为_________NA;若电池工作时消耗1mol二甲醚所能产生的最大电能为1320kJ,则该燃料电池的工作效率为________(燃烧电池的工作效率是指电池所能产生的最大电能与燃料燃烧时所能释放的全部热能之比)。