题目内容
若(NH4)2SO4在强热时分解的产物是SO2、N2、NH3和H2O则该反应中化合价发生变化和未发生变化的N原子数之比为
| A.1:4 | B.1:2 | C.2:1 | D.4:1 |
B
解析试题分析:利用化合价升降法将该氧化还原反应方程式配平,反应方程式为
3(NH4)2SO4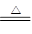 3SO2+N2+4NH3+6H2O,该反应中铵根离子和氨气分子中氮原子的化合价都是-3价,化合价不变,所以则该反应中化合价发生变化和未发生变化的N原子数之比为1:2,选B。
3SO2+N2+4NH3+6H2O,该反应中铵根离子和氨气分子中氮原子的化合价都是-3价,化合价不变,所以则该反应中化合价发生变化和未发生变化的N原子数之比为1:2,选B。
考点:考查氧化还原方程式的配平和计算。

下列说法正确的是
| A.氧化剂得电子数越多其氧化能力越强 | B.发生化学键断裂的过程不一定发生化学反应 |
| C.常温下所有的吸热反应都不能自发进行 | D.两种难溶物溶解度小的物质其Ksp一定也小 |
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体N2O4的混合气体1120mL(标准状况)。向反应后的溶液中加入1.0 mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
| A.该合金中铜与镁的物质的量之比是2:l |
| B.该浓硝酸中HN03的物质的量浓度是14.0 mol/L |
| C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL |
| D.NO2和N2O4的混合气体中,NO2的体积分数是80% |
工业上常利用反应 3Cl2 + 6KOH(热) → KClO3 + 5KCl + 3H2O 制取KClO3(混有KClO)。实
验室模拟上述制备:在含溶质14mol的KOH(aq,热)中通入一定量Cl2,充分反应后,测得
溶液中n(Cl-)=11mol;将此溶液低温蒸干,得到的固体中KClO3的物质的量可能为
| A.2.20 | B.2.33 | C.2.00 | D.0.50 |
有Fe2+、NO3-、Fe3+、NH4+、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
| A.氧化剂和还原剂的物质的量之比为1∶8 |
| B.该过程说明Fe(NO3)2溶液不宜加酸酸化 |
| C.每1 mol NO3-发生氧化反应,转移8 mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe2+-e-=Fe3+ |
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体a mol,向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO固体120g,若上述气体为NO,则a可能为 mol.
| A.2.50 | B.4.00 | C.7.50 | D.3.15 |
著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献。已知:金属铈(稀土元素在空气中易氧化变暗,受热时燃烧,遇水很快反应。(注:铈常见的化合价为+3和+4,氧化性Ce4+>Fe3+。)下列说法正确的是 ( )
| A.铈溶于氢碘酸的化学方程式可表示为:Ce+4HI=CeI4+2H2↑. |
| B.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+═Ce3++2Fe3+ |
| C.在一定条件下,电解熔融状态的CeO2制Ce,在阴极获得铈 |
| D.四种铈的核素13658Ce、13858Ce、14058Ce、14258Ce,它们互称为同素异形体 |
金属钾的冶炼可采用如下方法:2KF+CaC2 CaF2+2K↑+2C,下列有关说法合理的是( )
CaF2+2K↑+2C,下列有关说法合理的是( )
| A.该反应的氧化剂是KF,氧化产物是K |
| B.该反应能说明C的还原性大于K |
| C.电解KF溶液不可能制备金属钾 |
| D.CaC2、CaF2均为离子化合物,且阴、阳离子个数比均为2∶1 |