题目内容
【题目】已知2Fe2O3(s) +3C(s)=3CO2(g) +4Fe(s) △H=+468.2 kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
根据以上热化学方程式判断,下列说法正确的是 ( )
A. C(s)的燃烧热为393.5kJ
B. 右图可表示由C生成CO2的反应过程和能量关系
C. O2(g)与Fe(s)反应放出824.35kJ热量时,转移电子数为4NA
D. Fe2O3(s)+ ![]() C(g)=
C(g)= ![]() CO2(g)+2Fe(s) △H <234.1 kJ/mol
CO2(g)+2Fe(s) △H <234.1 kJ/mol
【答案】D
【解析】A. C(s)的燃烧热为393.5kJ/mol,故A错误;B. C生成CO2的反应需要加热条件以提高反应物的能量,右图不能表示由C生成CO2的反应过程和能量关系,故B错误;C. 将上述两个反应的热化学方程式相加减可得4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1648.7kJ/mol,所以O2(g)与Fe(s)反应放出824.35kJ热量时,转移电子数为6NA,故C错误;D. 因为Fe2O3(s)+ ![]() C(s)=
C(s)= ![]() CO2(g)+2Fe(s) △H=+234.1kJ/mol C(s)=C(g) △H>0,所以Fe2O3(s)+
CO2(g)+2Fe(s) △H=+234.1kJ/mol C(s)=C(g) △H>0,所以Fe2O3(s)+ ![]() C(g)=
C(g)= ![]() CO2(g)+2Fe(s) △H <234.1 kJ/mol。故D正确。故选D。
CO2(g)+2Fe(s) △H <234.1 kJ/mol。故D正确。故选D。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是__________________________。
(2)实验①和②的目的是_____________________。实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是_____________________。
(3)写出实验③的化学反应方程式:______________。
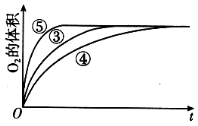
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。分析如图能够得出的实验结论是____________________________。