题目内容
10.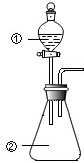 用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )| 选项 | ①中物质 | ②中物质 | 预测中的现象 |
| A | 稀盐酸 | 碳酸钠、氢氧化钠混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
| C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
| D | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.稀盐酸先和NaOH反应生成氯化钠和水,然后再和碳酸钠反应生成碳酸氢钠,最后碳酸氢钠和稀盐酸反应生成二氧化碳;
B.常温下,浓硝酸和铝发生钝化现象;
C.NaOH过量,开始不生成沉淀;
D.发生氧化还原反应.
解答 解:A.先发生盐酸与NaOH的反应,然后盐酸与碳酸钠反应生成碳酸氢钠,最后盐酸与碳酸氢钠反应生成气体,则现象不合理,故A错误;
B.常温下,Al遇浓硝酸发生钝化,则不能观察到红棕色气体,现象不合理,故B错误;
C.NaOH过量,开始不生成沉淀,反应生成偏铝酸钠和氯化钠,开始无现象,故C错误;
D.草酸与高锰酸钾发生氧化还原反应,溶液褪色,现象合理,故D正确;
故选D.
点评 本题考查物质的性质及实验装置的综合应用,为高频考点,把握物质的性质、发生的反应、反应与现象的关系为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.

练习册系列答案
相关题目
18.NA表示阿伏加德罗常数,以下说法中正确的是( )
| A. | 0.1mol钠离子含有电子数为1.1NA | |
| B. | 在常温常压下,1mol氩气含有的原子数为2NA | |
| C. | 1molNa2O2中含有离子数为3NA | |
| D. | 1molCCl2F2中含有氯气分子数为NA |
5.短周期主族元素X、Y、Z、W原子序数依次增大,X原子最外层有6个电子,Y是至今发现的非金属性最强的元素,Z在周期表中处于周期序数等于族序数的位置,W的单质广泛用作太阳能电池材料和电脑芯片.下列叙述正确的是( )
| A. | 原子半径由大到小的顺序:W>Z>Y>X,简单离子半径由大到小的顺序:X>Y>Z | |
| B. | 原子最外层电子数由多到少的顺序:Y>X>W>Z,最高正价由高到低顺序:W>Z | |
| C. | 元素非金属性由强到弱的顺序:Z>W>X,W的单质常温下可与氢氧化钠溶液反应 | |
| D. | 简单气态氢化物的稳定性由强到弱的顺序:X>Y>W |
15.红热的木炭与浓硝酸共热产生的气体等分为①和②两份,第①份先通过适量蒸馏水,再导入少量石灰水;第②份直接通入少量石灰水.则石灰水的变化最可能为( )
| A. | ①不变浑浊,②变乳白色 | B. | ①变乳白色,②不变浑浊 | ||
| C. | ①变乳白色,②变乳白色 | D. | ①不变浑浊,②不变浑浊 |
20.除去下列物质中所含的杂质,选用的实际正确的是( )
| 选项 | 物质(杂质) | 试剂 |
| A | 食盐(细沙) | NaOH溶液 |
| B | CO(NH3) | 浓H2SO4 |
| C | CO2(SO2) | Na2CO3溶液 |
| D | NaHCO3溶液(Na2CO3) | Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
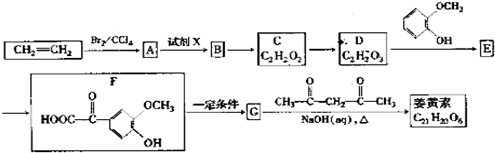

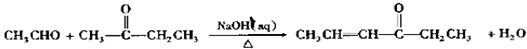

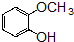 +OHCCOOH→
+OHCCOOH→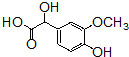 ,其反应类型是加成反应.
,其反应类型是加成反应.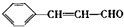 ),写出制备肉桂醛所需有机物的结构简式C6H5CHO、CH3CHO.
),写出制备肉桂醛所需有机物的结构简式C6H5CHO、CH3CHO.