题目内容
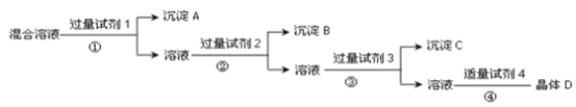
【题目】现有NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-,SO42-和NO3-的相互分离,实验过程如下:
请回答下列问题:
(1)写出上述实验过程中所用试剂的名称:试剂1为 ___,试剂2为___,试剂4为_________。
(2)加入过量试剂3的目的是_________ 。
(3)在加入试剂4后,获得晶体D的实验操作④的名称是_______。
【答案】BaCl2或Ba(NO3)2溶液 AgNO3溶液 稀HNO3 除去溶液中过量的Ba2+、Ag+ 蒸发浓缩、冷却结晶、过滤
【解析】
要实现Cl-、SO42-、NO3-的相互分离,通常用AgNO3沉淀Cl-,用BaCl2或Ba(NO3)2沉淀SO42-。若先加入AgNO3溶液,就会同时生成Ag2SO4和AgCl沉淀,因此应先加入过量的BaCl2或Ba(NO3)2溶液,即试剂1是BaCl2或Ba(NO3)2溶液,生成BaSO4沉淀即沉淀A,然后在滤液中加入过量的AgNO3溶液即试剂2,使Cl-全部转化为AgCl沉淀即沉淀B,在所得滤液中加入过量的Na2CO3即试剂3,使溶液中的Ag+、Ba2+完全形成沉淀,最后所得溶液为NaNO3和Na2CO3的混合物,再加入稀HNO3即试剂4,最后将溶液进行蒸发操作可得固体NaNO3,以此分析解答。
根据上述分析可知:试剂1是BaCl2或Ba(NO3)2溶液,沉淀A是BaSO4;试剂2是AgNO3溶液,沉淀B是AgCl,试剂3是Na2CO3溶液,沉淀C是Ag2CO3、BaCO3,试剂4是稀HNO3,晶体D是NaNO3。
(1)根据上述分析可知:试剂1为BaCl2或Ba(NO3)2溶液,试剂2为AgNO3溶液,试剂3为Na2CO3溶液,试剂4为稀HNO3;
(2)在加入过量的BaCl2或Ba(NO3)2后过滤除去BaSO4沉淀,在滤液中加入过量的AgNO3溶液,使Cl-全部转化为AgCl沉淀,反应后溶液中存在过量的Ag+、Ba2+,在所得滤液中加入过量的Na2CO3,能够使溶液中的Ag+、Ba2+完全沉淀;
(3)在加入过量稀硝酸后的溶液NaNO3溶液,由于NaNO3的溶解度受温度的影响变化较大,所以要从其溶液中获得溶质,应将溶液进行蒸发浓缩,然后冷却结晶、最后过滤可得NaNO3晶体,故获得晶体D的实验操作④的名称是蒸发浓缩、冷却结晶、过滤。