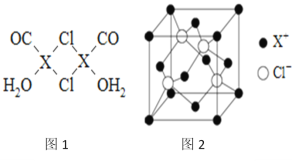
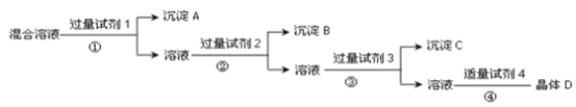
��Ŀ����
����Ŀ��O2��O3����Ԫ�ص����ֵ��ʣ����������ʽ������и��⣺
(1)��������O2��O3�������Ӹ�����Ϊ____��ԭ�Ӹ�����Ϊ_____�����ӵ����ʵ���֮��Ϊ____��
(2)���µ�ѹ�£��������O2��O3�������Ӹ�����Ϊ___��ԭ�Ӹ�����Ϊ_____��������Ϊ___��
(3)��NAΪ�����ӵ���������ֵ�����a g�����к��еķ�����Ϊb����c g�����ڱ�״���µ����Լ��__(�ú�NA��ʽ�ӱ�ʾ)��
(4)����100 mL 1 mol/L��ϡH2SO4��Һ����Ҫ����Ͳ��ȡŨH2SO4(�ܶ�Ϊ1.84 g��mL��1����������Ϊ98%)�����Ϊ____ mL��
���𰸡�3��2 1��1 3��2 1��1 2��3 2��3 ![]() 5.4
5.4
��������
(1)����n=![]() ��N=
��N=![]() NA�������ӹ��ɼ��㣻
NA�������ӹ��ɼ��㣻
(2)ͬ��ͬѹ�£�����Ħ�������ͬ��N=![]() NA��m=
NA��m=![]() M�����ӹ��ɼ��㣻
M�����ӹ��ɼ��㣻
(3)����£�����Ħ�������22.4L/mol��ag�����к��еķ�����Ϊb����������Ħ������=![]() g/mol��V=nVm��
g/mol��V=nVm��
(4)����ϡ��ǰ�����ʵ����ʵ����������Ũ����������
(1)��������Ϊm����������O2��O3�������Ӹ�����=![]() NA:
NA:![]() NA=3:2��һ�����������к���2����ԭ�ӣ�һ�����������к���3����ԭ�ӣ���������ԭ�Ӹ���=(3��2):(2��3)=1:1�������ʵ���֮��=
NA=3:2��һ�����������к���2����ԭ�ӣ�һ�����������к���3����ԭ�ӣ���������ԭ�Ӹ���=(3��2):(2��3)=1:1�������ʵ���֮��=![]() :
:![]() =3:2��
=3:2��
(2)��ͬѹ�£�����Ħ�������ͬ������N=![]() NA֪���������O2��O3�������Ӹ�������1:1��һ�����������к���2����ԭ�ӣ�һ�����������к���3����ԭ�ӣ�����ԭ�Ӹ���֮����2:3������m=
NA֪���������O2��O3�������Ӹ�������1:1��һ�����������к���2����ԭ�ӣ�һ�����������к���3����ԭ�ӣ�����ԭ�Ӹ���֮����2:3������m=![]() M֪��������֮�ȵ�����Ħ������֮��=32g/mol:48g/mol=2:3��
M֪��������֮�ȵ�����Ħ������֮��=32g/mol:48g/mol=2:3��
(3)������Ħ������ΪM=![]() =
=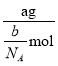 =
=![]() g/mol����cgO2�ڱ�״�������Ϊ��V=
g/mol����cgO2�ڱ�״�������Ϊ��V=![]() Vm=
Vm=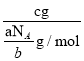 ��22.4L/mol=
��22.4L/mol=![]() L
L
(4)��ŨH2SO4�����ʵ���Ũ��Ϊ��c=![]() =
=![]() mol/L=18.4mol/L����ϡ�Ͷ��ɵã�100mL��1mol/L=18.4mol/L��V����ã�V=5.4mL��
mol/L=18.4mol/L����ϡ�Ͷ��ɵã�100mL��1mol/L=18.4mol/L��V����ã�V=5.4mL��

����Ŀ����һ���ݻ�Ϊ2L���ܱ������г���2mol NH3��3 mol O2���ں��ºʹ��������·�����Ӧ��4NH3(g)��5O2(g)4NO(g) + 6H2O(l) ������5min��ﵽƽ��״̬����ʱ��c(NH3)��c(O2)=4��7����
(1)��Ӧ��ʼ��ƽ��ʱ����NO��Ũ�ȱ仯��ʾ�÷�Ӧ��ƽ������v(NO)��__________��
(2)��ʼ״̬��ƽ��״̬�����ڵ�ѹǿ֮��Ϊ______��
(3)�������·�Ӧһ��ʱ�䣬������˵����Ӧ�ﵽƽ��״̬����___________ ��
A.c(H2O)���ֲ����״̬ B.�����ѹǿ���ֲ����״̬
C.4v��(NH3)=5v��(O2) D.NH3��O2Ũ��֮�ȱ��ֲ����״̬
(4)Ϊ���о�����ͭ�����������������ʵ�Ӱ�죬ijͬѧ���������һϵ�е�ʵ�飺�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���������У��ռ����������壬��¼�����ͬ�������������ʱ�䡣
A | B | C | D | E | F | |
4mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
����CuSO4��Һ(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
������ɴ�ʵ����ƣ����У�V1 = _________ ��V6 = _________ ��
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߣ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ��______________ ��