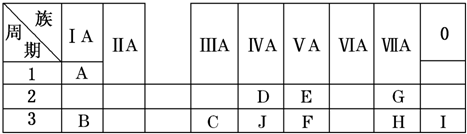
题目内容
2.Na和Na+两种粒子中,不相同的是( )①核内质子数 ②核外电子数 ③最外层电子数 ④核外电子层数.
| A. | ①② | B. | ③④ | C. | ①②③ | D. | ②③④ |
分析 根据原子转化成离子时核外电子层排布发生的变化进行分析解答本题,钠原子失去一个电子变成钠离子.
解答 解:Na失去一个电子变为Na+,最外层电子数由1个变成8个,电子层数由3个变成2个,核外电子数由11个变成10个,原子变成离子,变化的是核外电子数,和核外电子数变化导致变化的电子层数和最外层电子数,不变的是核内质子数,
故选D.
点评 本题主要考查了钠的两种不同微粒的区别,原子变成离子时,变化的量为核外电子数和电子层数,不变的量为质子数,也可根据原子结构示意图分析解答,难度不大.

练习册系列答案
相关题目
12.一定能在下列溶液中大量共存的离子组是( )
| A. | 水电离产生的H+浓度为1×10-12mol•L-1的溶液:NH4+、Na+、C1-、HCO3- | |
| B. | 含有大量Fe3+的溶液:SCN-、I-、K+、Br- | |
| C. | 能使pH试纸变蓝色的溶液:Na+、S2-、CO32-、AlO2- | |
| D. | 澄清透明的无色溶液:ClO-、MnO4-、A13+、SO42- |
13.A气体的水溶液呈酸性,若将A通入酸性的KMnO4溶液中,则紫红色褪色;若将A通入Br2水中,则Br2褪色并出现浑浊,则A气体是( )
| A. | Cl2 | B. | SO2 | C. | H2S | D. | CO2 |
7.元素周期表是化学学习和科学研究的重要工具,下列对于元素周期表的使用方法不正确的是( )
| A. | 为新元素的发现及预测它们的原子结构和性质提供线索 | |
| B. | 利用元素周期表发现元素的种类和原子的种类相同 | |
| C. | 在周期表中金属与非金属的分界处,可寻找半导体材料 | |
| D. | 指导人们在过渡元素中寻找催化剂和耐高温.耐腐蚀的合金材料 |
14.下列叙述中,正确的是( )
| A. | 两种原子,如果核外电子排布相同,则一定属于同种元素 | |
| B. | 两种微粒,若质量数不同,则其化学性质一定不同 | |
| C. | 两种微粒,若质量数相同,则其化学性质一定相同 | |
| D. | 微粒的核外电子数相同,则一定属于同种元素 |
11. 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一是芥子醇,结构简式如图所示.下列有关芥子醇的说法正确的是( )| A. | 芥子醇的分子式是C11H14O4,属于芳香烃 | |
| B. | 芥子醇分子中所有碳原子不可能在同一平面上 | |
| C. | 芥子醇不能使酸性KMnO4溶液褪色 | |
| D. | 芥子醇可以发生氧化反应、取代反应、加成反应 |
2.下列措施对增大反应速率明显有效的是( )
| A. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| B. | Fe与稀硫酸反应制取H2时,改用浓硫酸 | |
| C. | Al在氧气中燃烧生成A12O3,将Al片改成Al粉 | |
| D. | Na与水反应时增大水的用量 |