题目内容
下列有关生活生产中的叙述合理的是( )
| A.硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率。 |
| B.打开啤酒瓶的瓶盖,大量的气泡冒出来,该现象不能用勒夏特列原理解释。 |
| C.氯碱工业:用离子交换膜电解槽电解时,往阳极室注入经过精制的 NaCl溶液,往阴极室注入稀氢氧化钠溶液(或去离子水)。 |
| D.工业上合成氨采用500℃左右的温度,其原因是适当加快NH3的合成速率,催化剂在500℃左右时其活性最好,且能提高H2的转化率。 |
C
A:硫酸工业中SO2转化为SO3时采用常压,是因为在常压下,反应物的转化率已经相当高,再增大压强只会增加消耗,但SO2的转化率提高不大;B:啤酒溶液中存在下列平衡:CO2(aq) CO2(g),打开瓶盖,平衡向生成CO2气体的方向移动;D:催化剂只能提高反应速率,但不是不能提高H2的转化率,所以正确选项为C
CO2(g),打开瓶盖,平衡向生成CO2气体的方向移动;D:催化剂只能提高反应速率,但不是不能提高H2的转化率,所以正确选项为C
 CO2(g),打开瓶盖,平衡向生成CO2气体的方向移动;D:催化剂只能提高反应速率,但不是不能提高H2的转化率,所以正确选项为C
CO2(g),打开瓶盖,平衡向生成CO2气体的方向移动;D:催化剂只能提高反应速率,但不是不能提高H2的转化率,所以正确选项为C
练习册系列答案
相关题目
 2NH3(g);△H<0
2NH3(g);△H<0 2SO2(g)+O2(g);△H>0
2SO2(g)+O2(g);△H>0 2NO2(g),不能说明该反应已达到平衡状态的是( )
2NO2(g),不能说明该反应已达到平衡状态的是( )  2SO3(g)。
2SO3(g)。
 2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。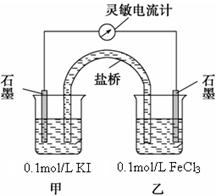
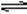 2 NH3达到平衡的标志是( )
2 NH3达到平衡的标志是( )
 109
109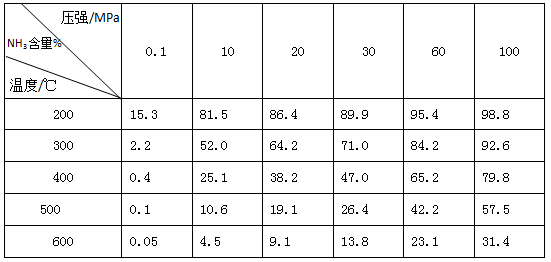
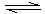 NH3的△H 0(填“>”、“<”或“无法判断”
NH3的△H 0(填“>”、“<”或“无法判断”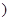 ,请简要说明理由 ;
,请简要说明理由 ; CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)
CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)  2Z3(g) 达到化学平衡状态后,采取下列措施平衡不会发生移动的是
2Z3(g) 达到化学平衡状态后,采取下列措施平衡不会发生移动的是