题目内容
【题目】下列化学用语表示或描述不正确的是
A. Ca的电子排布式是[Ar]3d2
B. BF3 的VSEPR的模型名称是平面三角形
C. NH4+中心原子N上的孤电子对数为0
D. 在[Cu(NH3)4]2+里,NH3的氮原子给出孤电子对,形成配位键
【答案】A
【解析】
A. Ca的电子排布式是1s22s22p63s23p64s2或[Ar]4s2,故A错误;
B. 价层电子对数=σ键电子对数+孤电子对数,根据BF3的电子式![]() 可知,中心原子B有没有孤电子对,有3个σ键电子对,共3个价层电子对,VSEPR模型名称为平面三角形,故C正确;
可知,中心原子B有没有孤电子对,有3个σ键电子对,共3个价层电子对,VSEPR模型名称为平面三角形,故C正确;
C. NH4+的电子式为![]() ,中心原子N上的孤电子对数为0,故C正确;
,中心原子N上的孤电子对数为0,故C正确;
D. NH3的电子式为![]() ,所以在[Cu(NH3)4]2+里,NH3的氮原子给出孤电子对,形成配位键,故D正确;
,所以在[Cu(NH3)4]2+里,NH3的氮原子给出孤电子对,形成配位键,故D正确;
综上所述,本题正确答案为A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
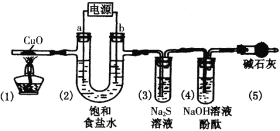
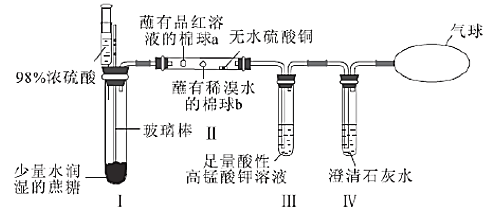
【题目】某同学设计了蔗糖与浓硫酸反应的改进装置,并对气体产物进行检验,实验装置如图所示。下列结论中正确的是( )
选项 | 现象 | 结论 |
A. | Ⅰ中注入浓硫酸后,可观察到试管中白色固体变为黑色 | 体现了浓硫酸的吸水性 |
B. | Ⅱ中观察到棉球a、b都褪色 | 均体现了SO2的漂白性 |
C. | Ⅱ中无水硫酸铜变蓝 | 说明反应产物中有H2O |
D. | Ⅲ中溶液颜色变浅,Ⅳ中澄清石灰水变浑浊 | 说明有CO2产生 |
A.AB.BC.CD.D