题目内容
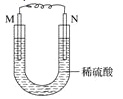
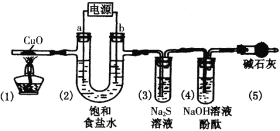
【题目】用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)并进行相关实验(装置如图),电解一段时间后,各部分装置及对应的现象为:(1)中黑色固体变红;(2)电极a附近溶液出现浑浊;(3)中溶液出现浑浊;(4)中溶液红色褪去。下列对实验现象解释不正确的是
A.(1)中:CuO+H2![]() Cu+H2O
Cu+H2O
B.(2)中a电极:2H2O+2e-=H2↑+2OH-,Mg2++2OH-=Mg(OH)2↓
C.(3)中:Cl2+S2-=S↓+2Cl-
D.(4)中:Cl2具有强氧化性
【答案】D
【解析】
用惰性电极电解饱和食盐水(含少量Ca2+、Mg2+)产生的气体为氢气和氯气,氯气具有强氧化性,而氢气在加热条件下具有较强还原性,根据(1)中黑色固体变红,(2)电极a附近溶液出现浑浊可知,a电极为阴极,放出氢气,生成氢氧根与镁离子结合成白色沉淀,b电极为阳极,产生的氯气可氧化硫化钠生成硫沉淀出现浑浊,过量的氯气通入含酚酞的NaOH溶液中,溶液褪色的原因可能为H+中和了OH-,也可能是氯气与水反应生成的次氯酸的强氧化性所致,据此分析解答。
A.(1)中黑色固体变红,是氢气还原氧化铜,反应的化学方程式为:CuO+H2![]() Cu+H2O,故A正确;
Cu+H2O,故A正确;
B.(2)电极a附近溶液出现浑浊,则a电极放出氢气生成氢氧根,与镁离子结合成白色沉淀,相关反应为:2H2O+2e-═H2↑+2OH-,Mg2++2OH-═Mg(OH)2↓,故B正确;
C.(3)中溶液出现浑浊,是产生的氯气氧化硫化钠生成硫沉淀,离子方程式为:Cl2+S2-═S↓+2Cl-,故C正确;
D.(4)中过量的氯气通入含酚酞的NaOH溶液中,溶液褪色的原因可能为H+中和了OH-,也可能是氯气与水反应生成的次氯酸的强氧化性所致,故D错误;
故选D。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】现向下列装置中缓慢通入气体X,分别进行关闭和打开活塞K的操作,则品红溶液和澄清石灰水中现象相同的一组是
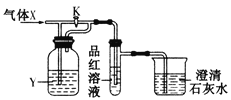
选项 | A | B | C | D |
X | NO2 | SO2 | Cl2 | CO2 |
Y(过量) | 浓H2SO4 | NaHCO3饱和溶液 | Na2SO3溶液 | NaHSO3饱和溶液 |
A.AB.BC.CD.D
【题目】根据实验操作及现象所得出的解释或结论不正确的是( )
选项 | 实验操作及现象 | 解释或结论 |
A. | 向某溶液中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,有白色沉淀产生 | 该溶液中一定含有SO |
B. | 向某溶液中加入浓NaOH溶液,加热,产生 能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中一定含有NH |
C. | 向某钾盐中滴加盐酸,产生使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3或KHCO3 |
D. | 酸性硝酸铁溶液中加入几滴碘化钾淀粉溶液,出现蓝色 | 铁离子具有较强氧化性,将I-氧化生成I2 |
A.AB.BC.CD.D