题目内容
【题目】电讯器材元件材料MnCO3在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度变化如下图。下列说法不正确的是( )
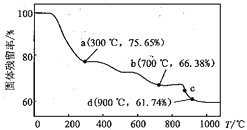
A. a 点剩余固体中n(Mn) : n(O) = 1 : 2
B. b 点对应固体的成分为Mn3O4
C. c 点发生的反应为2MnO2 △ 2MnO+O2↑
D. d 点对应固体的成分为MnO
【答案】C
【解析】A、设MnCO3的物质的量为1 mol,即质量为115 g,a点剩余固体质量为115 g×75.65%=87 g,减少的质量为115 g-87 g=28 g,可知MnCO3失去的组成为CO,故剩余固体的成分为MnO2,剩余固体中n(Mn) : n(O) = 1 : 2,选项A正确;B、b点剩余固体质量为115 g×66.38%=76.337 g,因m(Mn)=55g,则m(O )2=76.337 g-55 g=21.337 g,则n(Mn)∶n(O)= ![]() ∶
∶![]() =3∶4,故剩余固体的成分为Mn3O4,选项B正确;D、d点剩余固体质量为115 g×61.74%=71 g,据锰元素守恒知m(Mn)=55g,则m(O )1=71g-55g=16g,则n(Mn)∶n(O)=
=3∶4,故剩余固体的成分为Mn3O4,选项B正确;D、d点剩余固体质量为115 g×61.74%=71 g,据锰元素守恒知m(Mn)=55g,则m(O )1=71g-55g=16g,则n(Mn)∶n(O)= ![]() ∶
∶![]() =1∶1,故剩余固体的成分为MnO,C、因c点介于b、d之间,故c点对应固体的成分为Mn3O4与MnO的混合物。发生的反应为2Mn3O4 △ 6MnO+O2↑,选项C不正确。答案选C。
=1∶1,故剩余固体的成分为MnO,C、因c点介于b、d之间,故c点对应固体的成分为Mn3O4与MnO的混合物。发生的反应为2Mn3O4 △ 6MnO+O2↑,选项C不正确。答案选C。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】短周期元素W、X 、Y 和Z 在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21 。回答下列问题:
W | X | |||
Y | Z |
(1)X 在元素周期表中的位置为_______。
(2)四种元素简单离子的半径由大到小为_____________(用离子符号表达)。
(3)W的最简单氢化物的电子式为________________。
(4)W、Z 最高价氧化物的水化物酸性较强的为___________(填化学式)。
(5)Y单质与Fe2O3 反应能放出大量的热,常用于焊接钢轨,该反应化学方程式为____________________。
(6)向盛有3 mL 鸡蛋清溶液的试管里滴入几滴W的最高价氧化物的水化物浓溶液,实验现象为________________________________________。
(7)C3H7Z 的结构简式有____________________。
(8)ZX2气体是一种广谱杀菌消毒剂。工业上可利用NaZX3和NaZ 在酸性条件下制得ZX2 同时得到Z元素的单质,该反应的离子方程式为_____________。
