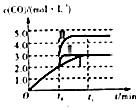题目内容
【题目】在溶液中,反应A+2BC分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L、c(B)=0.200mol/L 及 c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件.所改变的条件和判断的理由是:
②; .
③; .
(2)实验②平衡时B的转化率为;实验③平衡时C的浓度为;
(3)该反应的△H0,其判断理由是
(4)该反应进行到4.0min时的平均反应速率:
实验②:vB=
实验③:vc= .
【答案】
(1)加催化剂,达到平衡的时间缩短,平衡时A的浓度未变,温度升高,达到平衡的时间缩短,平衡时A的浓度减小
(2)40%,0.06mol/L
(3)>,温度升高,平衡向正反应方向移动
(4)0.014mol(L?min)﹣1,0.009mol(L?min)﹣1
【解析】解:(1)与①比较,②缩短达到平衡的时间,因催化剂能加快化学反应速度率,化学平衡不移动,所以②为使用催化剂;
与①比较,③缩短达到平衡的时间,平衡时A的浓度减小,因升高温度,化学反应速度率加快,化学平衡移动,平衡时A的浓度减小,
所以答案是:②加催化剂;达到平衡的时间缩短,平衡时A的浓度未变;③温度升高;达到平衡的时间缩短,平衡时A的浓度减小;
(2)由图可知,实验②平衡时A的浓度为0.06mol/L,故A的浓度变化量0.1mol/L﹣0.06mol/L=0.04mol/L,由方程式可知B的浓度变化量为0.04mol/L×2=0.08mol/L,故平衡时B的转化率为 ![]() ×100%=40%;
×100%=40%;
实验③平衡时A的浓度为0.04mol/L,故A的浓度变化量0.1mol/L﹣0.04mol/L=0.06mol/L,由方程式可知C的浓度变化量为0.06mol/L,故平衡时C的浓度为0.06mol/L,
所以答案是:40%;0.06mol/L;
(3)因③温度升高,平衡时A的浓度减小,化学平衡向吸热的方向移动,说明正反应方向吸热,即△H>0,
所以答案是:>;温度升高,平衡向正反应方向移动;
(4)实验②中,vA= ![]() =0.007mol(Lmin)﹣1,所以vB=2vA=0.014mol(Lmin)﹣1;
=0.007mol(Lmin)﹣1,所以vB=2vA=0.014mol(Lmin)﹣1;
实验③中,vA= ![]() =0.009mol(Lmin)﹣1,所以vC=vA=0.009mol(Lmin)﹣1,
=0.009mol(Lmin)﹣1,所以vC=vA=0.009mol(Lmin)﹣1,
所以答案是:0.014mol(Lmin)﹣1;0.009mol(Lmin)﹣1.
【考点精析】解答此题的关键在于理解化学平衡状态本质及特征的相关知识,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效),以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

【题目】下列图表中a、b、c表示对应装置的仪器中加入的试剂,可制取、净化、收集的气体是
选项 | a | b | c | 气体 | 装置 |
A | 浓氨水 | 生石灰 | 浓硫酸 | NH3 |
|
B | 浓H2SO4 | 铜屑 | NaOH溶液 | SO2 | |
C | 稀HNO3 | 铜屑 | H2O | NO | |
D | 稀盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | CO2 |
A. A B. B C. C D. D