题目内容
【题目】NA代表阿伏加德罗常数,下列叙述错误的是( )
A. 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B. 在H2O2+Cl2===2HCl+O2反应中,每生成32 g氧气,则消耗NA个Cl2分子
C. 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D. 一定温度下,1 L 0.50 mol·L-1 NaCl溶液与2 L 0.25 mol·L-1 Na2CO3溶液含Na+的物质的量不同
【答案】A
【解析】因为稀释以后,硫酸溶液的密度变小,![]() 硫酸)
硫酸)![]() 硫酸),而溶质硫酸的质量不变,故质量分数大于
硫酸),而溶质硫酸的质量不变,故质量分数大于![]() ,A错误;32 g氧气的物质的量为:
,A错误;32 g氧气的物质的量为: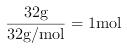 ,根据反应H2O2+Cl2===2HCl+O2可以知道,生成
,根据反应H2O2+Cl2===2HCl+O2可以知道,生成![]() 氧气消耗
氧气消耗![]() 氯气,即消耗NA个Cl2分子,B正确;标准状况下,分子数为NA的CO、C2H4混合气体物质的量为
氯气,即消耗NA个Cl2分子,B正确;标准状况下,分子数为NA的CO、C2H4混合气体物质的量为![]() ,气体体积约为22.4L,质量为:
,气体体积约为22.4L,质量为:![]() g,C正确;1 L、 0.50 mol·L-1 NaCl溶液中含有0.5mol钠离子,2 L 0.25 mol·L-1 Na2CO3溶液含Na+ 为1 mol,两溶液中含
g,C正确;1 L、 0.50 mol·L-1 NaCl溶液中含有0.5mol钠离子,2 L 0.25 mol·L-1 Na2CO3溶液含Na+ 为1 mol,两溶液中含![]() 的物质的量不同,D正确;正确选项A。
的物质的量不同,D正确;正确选项A。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案【题目】工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。反应原CH2=CH2(g)+H2O(g)=CH3CH2OH(g )△H。已知几种共价键的键能如下:
化学键 | C-H | C=C | H-O | C-C | C-O |
键能/kJ·mol-1 | 413 | 615 | 463 | 348 | 351 |
下列说法错误的是
A. 上述合成乙醇的反应原子利用率为100%
B. 相同时间段内,用该反应中三种物质表示的该反应的化学反应速率相等
C. 碳碳双键的键能大于碳碳单键键能,但碳碳单键更稳定
D. 上述反应式中,△H=+34kJ·mol-1

