题目内容
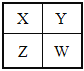
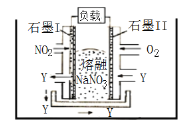
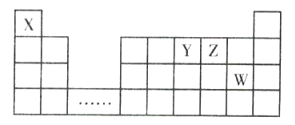
【题目】X、Y、Z、W四种短周期元素,它们在周期表中的位置如图所示,下列说法正确的是( )
A.四种元素的原子半径由小到大的顺序为r(X)<r(Z)<r(W)<r(Y)
B.X、Y、Z既能形成离子化合物,又能形成共价化合物
C.X与其余三种元素之间形成的核外电子总数为10的微粒只有2种
D.H2Z与HW所含的化学键类型不同
【答案】B
【解析】
根据元素周期表的结构可知,X为H,Y为N,Z为O,W为Cl。
A.H、N、O、W的原子半径顺序为r(H)<r(O)<r(N)<r(Cl),A错误;
B.H、N、O可以形成HNO3,HNO3属于共价化合物,可以形成NH4NO3,NH4NO3属于离子化合物,B正确;
C.构成的10电子微粒有NH3、NH4+、H2O、H3O+等,C错误;
D.H2Z为H2O,HW为HCl,二者均只含共价键,D错误;
故选B。

练习册系列答案
相关题目