题目内容
【题目】将1molNa和1molAl的混合物投入足量水中,产生气体在标准状况下的体积为 ( )
A. 11.2L B. 22.4L C. 33.6L D. 44.8L
【答案】D
【解析】
根据下面的化学反应方程式
2Na+2H2O=2NaOH=H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
可知:两金属恰好完全与水反应共产生:0.5+1.5=2mol的氢气,在标准状况下的体积为44.8L

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】海洋是一个巨大的化学资源宝库。海水综合利用的部分流程如下:

已知:Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。
(1)操作A是___________(填实验基本操作名称),粗盐中常含 Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、______ 、______、盐酸试剂来进行提纯。
(2)操作B需加入下列试剂中的一种,最合适的是______(选填编号)。
a.氢氧化钠溶液 b.澄清石灰水 c.石灰乳 d.碳酸钠溶液
(3)已知母液中的主要成分如下表:
离子 | Na+ | Mg2+ | Cl- | SO42- |
浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
理论上,1m3母液中最多可得到Mg(OH)2的质量为___________。
(4)利用下图所示装置模拟工业上从母液中提取溴,在B瓶中得到较浓的溴水。

实验方案为:关闭b、d,打开a、c,由a向A中缓慢通入________至反应完全,发生反应的的离子方程式是_________________________;再关闭a、c,打开b、d、e,由b向A中鼓入足量_________,同时由 e 向B中通入足量_________;关闭b、e,打开a,再由a 向B中缓缓鼓入足量___________,即可在B中得到较浓的溴水。(本实验中须使用的试剂有:SO2、Cl2、热空气) 。
【题目】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。请回答下列问题。
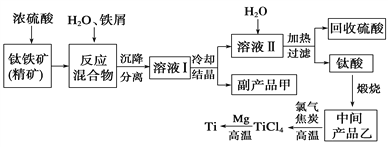
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C═2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______________;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为____________________。
(2)上述生产流程中加入铁屑的目的是_________________________,此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.0018mol/L,当溶液的pH等于_______时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为___________________________________________________________。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为________。Mg还原TiCl4过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是_________。除去所得金属钛中少量的金属镁可用的试剂是__________________。