题目内容
【题目】常温下有0.1 mol·L-1四种溶液NaOH、 NH3·H2O、 HCl 、CH3COOH
(1)已知CH3COOH溶液的pH=3,其电离度为 ,由水电离的c(H+)= mol·L-1。
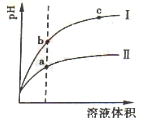
(2)相同pH的CH3COOH溶液和HCl溶液加水稀释,其pH变化情况如图,其中表示HCl溶液的是曲线 ,a、b两点中,导电能力更强的是 。
(3)NH3·H2O溶液和HCl溶液混合,已知体积V(NH3·H2O)> V(HCl),当溶液中c(NH3·H2O)= c(NH4+)时,溶液的pH= 。[已知:Kb(NH3·H2O)=1.77×10-5,lg 1.77=0.25]
【答案】(1)1%;1×10-11(2);a(3)9.25
【解析】
试题分析:(1)电离度=c(H+)÷c(CH3COOH)×100%=10-3÷0.1×100%=1%;由水电离的c(H+)等于溶液中氢氧根离子浓度=Kw÷c(OH-)=10-14÷10-3=1×10-11 mol/L。
(2)pH相等的醋酸和盐酸中,加水稀释促进醋酸电离,稀释相同的倍数后,醋酸中氢离子浓度大于盐酸,所以pH变化大的为强酸,根据图象知,I为盐酸;溶液的导电能力与离子浓度成正比,氢离子浓度越大溶液的pH越小,所以溶液导电能力较大的是a 。
(3)根据NH3·H2O![]() NH4++OH-,Kb=([NH4+]×[OH-])÷[NH3·H2O],则1.77×10-5=c(OH-),POH=5-lg 1.77= 4.75,所以溶液的pH=14-4.75=9.25.
NH4++OH-,Kb=([NH4+]×[OH-])÷[NH3·H2O],则1.77×10-5=c(OH-),POH=5-lg 1.77= 4.75,所以溶液的pH=14-4.75=9.25.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目