题目内容
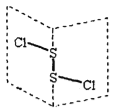
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体。下列说法错误的是( )
![]()
A. S2Cl2的电子式为
B. S2Cl2同时含有极性键和非极性键
C. S2Br2与S2Cl2结构相似,熔沸点:S2Br2 > S2Cl2
D. S2Cl2与H2O反应的化学方程式可能为: 2S2Cl2+2H2O = SO2↑+3S↓+4HCl
【答案】A
【解析】试题分析:A.二氯化二硫(S2Cl2)是共价化合物,由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S_2 Cl_2 的电子式为![]() ,每个原子周围都满足8电子稳定结构,错误;B.在S2Cl2分子中S-S为非极性键,S-Cl键为极性键,S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称,应为极性分子,正确;C.由于Cl、Br是同一主族的元素,S2Br2与S2Cl2结构相似组成与结构相似,相对分子质量越大,分子间作用力越强,熔沸点越高,则熔沸点:S2Br2 > S2Cl2,正确;D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),反应的方程式可能为2S2Cl2+2H2O = SO2↑+3S↓+4HCl,正确。
,每个原子周围都满足8电子稳定结构,错误;B.在S2Cl2分子中S-S为非极性键,S-Cl键为极性键,S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称,应为极性分子,正确;C.由于Cl、Br是同一主族的元素,S2Br2与S2Cl2结构相似组成与结构相似,相对分子质量越大,分子间作用力越强,熔沸点越高,则熔沸点:S2Br2 > S2Cl2,正确;D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),反应的方程式可能为2S2Cl2+2H2O = SO2↑+3S↓+4HCl,正确。

练习册系列答案
相关题目