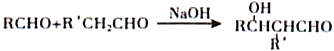题目内容
【题目】较活泼金属与硝酸反应,产物复杂。如一定浓度的硝酸与镁反应,可同时得到NO、NO2、N2三种气体。某同学欲用下列仪器组装装置来直接验证有NO、NO2生成并制取氮化镁。(假设实验中每步转化均是完全的)

已知:①NO2沸点是21.1℃、熔点是-11℃;NO的沸点是-151℃、熔点是-164℃;②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是(_____) (填序号)。
a. A→ D → C → F → B → F →E b. A→ C → D → F → B → F →E
c. A→ F → C → D → F → B →E d. A→ F → D → C → F → B →E
(2)确定还原产物中有NO2的现象是______________________________,实验中两次使用装置F,第二次使用装置F的作用是____________________________________。
(3)实验前需先打开开关K,向装置内通CO2气体,其目的是____________,当_______________时停止通入CO2。
(4)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式____________________________________________________。
(5)在A中反应开始时,某同学马上点燃B处的酒精灯,实验结束后通过测定发现B处的产品纯度不高,原因是______________________________________(用化学方程式回答)。
(6)验证B处有氮化镁生成的方法是_______________。
【答案】 a D中有红棕色液体生成 防止E中水蒸气进入B中,造成产物不纯 排除装置内空气,防止干扰实验 E中产生白色沉淀 5NO+3MnO4-+4H+=3Mn2++5NO3-+2H2O CO2+2Mg![]() 2MgO+C 取B中固体少量于试管中,向其中加入少量水,若产生能使湿润的红色石蕊试纸变蓝的气体,则B中有氮化镁生成
2MgO+C 取B中固体少量于试管中,向其中加入少量水,若产生能使湿润的红色石蕊试纸变蓝的气体,则B中有氮化镁生成
【解析】试题分析:本题考查Mg与HNO3反应产物的探究以及Mg3N2的制备,涉及装置的连接、物质的检验、方程式的书写。
(1)根据题意“一定浓度的硝酸与Mg反应可同时得到NO、NO2、N2”,若有NO2生成则气体呈红棕色,根据已知①NO2、NO的熔沸点,在装置D中可将NO2冷凝为液态,可观察到装置D中有红棕色液体生成;利用NO具有还原性,用装置C中酸性KMnO4溶液验证NO;根据已知②Mg3N2遇水会发生水解,与Mg反应的N2必须是干燥的,气体在进入装置B之前必须用浓硫酸干燥N2,且要防止H2O(g)进入制备Mg3N2的装置;装置的连接顺序为:A→D→C→F→B→F→E,答案选a。
(2)根据上述分析,确定还原产物中有NO2的现象是:装置D中有红棕色液体生成。Mg3N2遇水会发生水解,实验中两次使用装置F,第一次使用装置F的作用是:干燥N2;第二次使用装置F的作用是:防止E中H2O(g)进入B中,使Mg3N2不纯。
(3)由于NO能与O2反应生成NO2,会影响NO2、NO的验证,实验开始前要排出装置中空气,所以实验前先打开开关K,向装置内通CO2气体,其目的是:排除装置内空气,防止干扰实验;当观察到装置E的Ba(OH)2溶液中产生白色沉淀时,表明装置中空气已经排尽,停止通入CO2。
(4)装置D中观察到有红棕色液体出现,装置C中溶液颜色慢慢褪去,说明酸性KMnO4溶液将NO氧化成NO3-,同时MnO4-被还原成Mn2+,反应可写成NO+MnO4-→NO3-+Mn2+,N元素的化合价由+2价升至+5价,Mn元素的化合价由+7价降至+2价,根据得失电子守恒配平为5NO+3MnO4-→5NO3-+3Mn2+,结合原子守恒、电荷守恒,写出离子方程式为5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O。
(5)在A中反应开始时,马上点燃B处的酒精灯,Mg与CO2发生置换反应生成MgO和C,导致实验结束后B处制得的Mg3N2纯度不高,Mg与CO2反应的化学方程式为2Mg+CO2![]() 2MgO+C。
2MgO+C。
(6)Mg3N2遇水发生水解生成Mg(OH)2和NH3,检验有Mg3N2生成只要检验B处固体中加水产生NH3即可,验证B处有Mg3N2生成的方法是:取B中固体少量于试管中,向其中加入少量水,若产生能使湿润的红色石蕊试纸变蓝的气体,则B中有氮化镁生成。

 中考解读考点精练系列答案
中考解读考点精练系列答案