题目内容
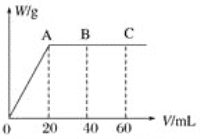
【题目】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答:
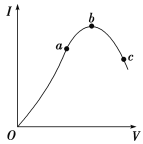
(1)“O”点导电能力为0的理由是_________________________。
(2)a、b、c三点处,溶液的c(H+)由小到大的顺序为____________。
(3)a、b、c三点处,电离程度最大的是________。
(4)若将c点溶液中c(CH3COO-)增大,c(H+)减小,可采取的措施是:
①____________________________________________________;
②___________________________________________________;
③___________________________________________________。
【答案】在“O”点处醋酸未电离,无离子存在c<a<bc加少量NaOH固体加少量Na2CO3固体加入Zn、Mg等金属
【解析】
溶液的导电性与离子浓度有关,离子浓度越大,导电性越强;导电能力越强,离子浓度越大,氢离子浓度越大;溶液越稀,越促进醋酸电离,则溶液中氢离子的物质的量越大,电离程度越大;使c(CH3COO-)增大,溶液c(H+)减小,可以加如碱、比醋酸弱的酸的盐、活泼金属等。
溶液的导电能力主要由离子浓度来决定,题目中的图象说明冰醋酸加水稀释过程中,离子浓度随着水的加入先逐渐增大到最大值又逐渐减小,故c(H+)在b点最大,c点最小,这是因为c(H+)=(n(H+))/(V(aq)),加水稀释,醋酸的电离平衡正向移动,n(H+)增大使c(H+)有增大的趋势,而V(aq)增大使c(H+)有减小的趋势,c(H+)是增大还是减小,取决于这两种趋势中哪一种占主导地位。在“O”点时,未加水,只有醋酸,因醋酸未发生电离,没有自由移动的离子存在,故不能导电;要使CH3COO-的浓度增大同时使H+浓度减小,可通过加入强碱、能与醋酸反应的盐、活泼金属等使醋酸的电离平衡正向移动。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案