题目内容
12.下列关于酸碱指示剂或pH试纸的说法正确的是( )| A. | 将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照 | |
| B. | 不能使无色酚酞试液变色的溶液是酸性溶液 | |
| C. | 可以用紫色石蕊试液作为强酸滴定强碱的指示剂 | |
| D. | 用pH试纸测定某溶液的pH=8.5,此溶液一定是某种碱的溶液 |
分析 A、用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照;
B、不能使无色酚酞试液变色的溶液是pH<10;
C、石蕊变色不明显;
D、pH试纸只能精确到1,且溶液显碱性的溶液不一定是碱溶液.
解答 解:A、将一小块干燥的试纸放在表面皿上,用干燥的玻璃棒蘸取少量待测液点在试纸中部,然后与标准比色卡对照,故A正确;
B、不能使无色酚酞试液变色的溶液是pH<10,故可能是酸性溶液,也可能是中性或弱碱性溶液,故B错误;
C、石蕊变色不明显,不能用作中和滴定指示剂,故C错误;
D、pH试纸只能精确到1,故不能测得溶液的pH为8.5,且溶液显碱性的溶液不一定是碱溶液,可能是强碱弱酸盐溶液,故D错误.
故选A.
点评 本题考查了溶液的pH的计算,应注意的是溶液显碱性的溶液不一定是碱溶液,可能是强碱弱酸盐溶液.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
2.下列关于反应热的说法不正确的是( )
| A. | 已知下列热化学方程式:2H2(g)+O2(g)═2H2O(g)△H=-484kJ•mol-1,则氢气的燃烧热为242kJ•mol-1 | |
| B. | 中和反应的实质是H+ 与OH-结合生成水,若有其它物质生成,这部分反应热不在中和热内 | |
| C. | 物质的燃烧热可利用仪器由实验测得 | |
| D. | 中和热不包括物质溶解、电离、水合等过程中的热效应 |
17.关于浓H2SO4、稀H2SO4的叙述中正确的是( )
| A. | 浓H2SO4、稀H2SO4都难挥发 | |
| B. | 浓H2SO4、稀H2SO4都有氧化性,故浓H2SO4、稀H2SO4都是氧化性的酸 | |
| C. | 浓H2SO4、稀H2SO4在加热时都能与铜反应 | |
| D. | 浓H2SO4、稀H2SO4在常温下都能用铁制容器贮存 |
4.A、B、C、D、E是中学化学中五种常见元素,有关信息如下:
请回答下列问题:
(1)A的氢化物分子式是NH3,用电子式表示该物质的形成过程为: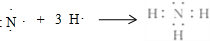 .写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
.写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生).
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:①③ ①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏.
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子式是NH3,用电子式表示该物质的形成过程为:
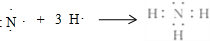 .写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
.写出实验室制取该物质的化学方程式Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.(2)A、D的氢化物相互反应,产生白色固体,对该固体中阳离子存在检验的操作方法是:取该白色固体少许于试管中,加入适量浓NaOH溶液并加热,用湿润的红色石蕊试纸接近试管口检验放出的气体,若试纸变蓝(或用蘸有浓盐酸的玻璃棒靠近试管口,有白烟产生).
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有:①③ ①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏.
1.环癸五烯的结构简式可表示为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 根据 的结构特点可知环癸五烯的分子式为C10H8 的结构特点可知环癸五烯的分子式为C10H8 | |
| B. | 常温常压下环癸五烯是一种易溶于水的无色气体 | |
| C. | 环癸五烯既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| D. | 乙烯和环癸五烯互为同系物 |
2.碳酸钠(Na2CO3)俗称纯碱,是一种重要的基础化工原料,广泛应用于玻璃、造纸等工业.下列与碳酸钠有关的说法正确的是( )
| A. | Na2CO3的稳定性介于Na2CO3•10H2O和NaHCO3之间 | |
| B. | “侯氏制碱法”制得的碱是指NaHCO3 | |
| C. | 可用盐酸鉴别Na2CO3 和NaHCO3固体 | |
| D. | 纯碱有时可代替烧碱使用,比如溶解石英、吸收氯气等 |
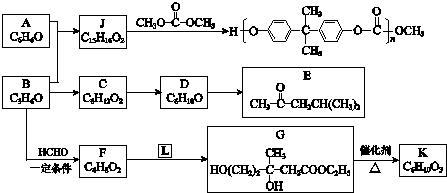
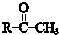 +
+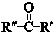 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$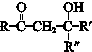 (R、R′、R″为氢原子或烃基)
(R、R′、R″为氢原子或烃基) .
. .
. .F和L反应生成G是加成反应,L的结构简式CH3COOCH2CH3.
.F和L反应生成G是加成反应,L的结构简式CH3COOCH2CH3. .
. .
.
 .
. .
.