题目内容
3.下列操作达不到预期目的是( )①石油分馏时把温度计插入受热的液体中
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用溴乙烷与氢氧化钠溶液加热制取乙烯
④将苯和溴水混合后加入铁粉制取溴苯
⑤将敞口久置的电石与蒸馏水混合制乙炔.
| A. | 只有①⑤ | B. | 只有③④⑤ | C. | 只有①②③⑤ | D. | ①②③④⑤ |
分析 ①石油分馏时把温度计测量馏分温度;
②酸性高锰酸钾溶液和乙炔、H2S都发生氧化还原反应;
③溴乙烷与NaOH水溶液发生取代反应;
④将苯和溴混合后加入铁粉制取溴苯;
⑤将敞口久置的电石与蒸馏水混合制乙炔时不能收集到乙炔.
解答 解:①石油分馏时把温度计测量馏分温度,所以温度计水银球位于蒸馏烧瓶支管口处,故错误;
②酸性高锰酸钾溶液和乙炔、H2S都发生氧化还原反应,所以不能用酸性高锰酸钾溶液除去乙炔中的硫化氢,可以用碱溶液除去硫化氢,故错误;
③溴乙烷与NaOH水溶液发生取代反应生成乙醇,故错误;
④将苯和溴混合后加入铁粉制取溴苯,苯和溴水不反应,故错误;
⑤将敞口久置的电石与蒸馏水混合制乙炔时,因为敞口所以不能收集到乙炔,故错误;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及除杂、气体的收集、气体的制备、实验操作等知识点,明确实验原理是解本题关键,注意从实验操作的规范性及评价性进行分析判断,易错选项是④.

练习册系列答案
相关题目
14.某温度下,100mL 0.4mol/L醋酸溶液与足量Zn粒反应生成H2的速率v(H2)=0.01mol/(L•min).为了减缓反应速率,但又不影响生成H2的总量,下列有关说法正确的是( )
| A. | 可向该溶液中加少量CaCO3固体 | |
| B. | 可向该溶液中加入10 mL 0.1 mol/L醋酸溶液 | |
| C. | 可向该溶液中加入少量NaNO3溶液 | |
| D. | 若向该溶液中加入少量醋酸钠固体,反应速率可能变成v(H2)=0.3 mol/(L•h) |
8.下列各表述与示意图一致的是( )
| A. |  表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. |  图中曲线表示反应2SO2 (g)+O2 (g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 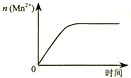 表示10 mL 0.01 mol•L-1KMnO4 酸性溶液与过量的0.1 mol•L-1H2 C2 O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 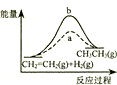 图中a、b曲线分别表示反应CH2=CH2 (g)+H2 (g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
15.元素的种类比核素的种类( )
| A. | 多 | B. | 少 | C. | 相等 | D. | 不能确定 |
12.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 双氧水催化分解 | B. | 乙醇燃烧 | ||
| C. | 铝粉与氧化铁粉末反应 | D. | 氯化铵与氢氧化钡晶体反应 |
13.一定温度下,下列溶液的离子浓度关系式正确的是( )
| A. | pH=5的H2S溶液中:c(OH-)+c(HS-)=1×10-5mol•L-1 | |
| B. | pH相同的①NH4F ②NH4Cl ③NH4Al(SO4)2三种溶液的物质的量浓度 ①>②>③ | |
| C. | pH=2 的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-) | |
| D. | pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 |