题目内容
【题目】NA是阿伏加德罗常数的值。下列说法正确的是( )
A.常温下,pH=12的氢氧化钠溶液中含有OH- 数目为0.01 NA
B.22.4 L(标准状况)氩气含有的质子数为18NA
C.92.0 g甘油(丙三醇)中含有羟基数为1.0NA
D.含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023
【答案】B
【解析】
A. 缺少溶液的体积,无法计算常温下pH=12的氢氧化钠溶液中含有OH- 数目,故A错误;
B. 氩原子的质子数为18,22.4 L(标准状况)氩气含有的质子数为18NA,故B正确;
C.92.0g甘油(丙三醇)的物质的量为92g÷92g·mol-1=1mol,1mol丙三醇含有3mol羟基,即含有羟基数为3.0NA,故C错误;
D. 2H2SO4(浓)+Cu![]() CuSO4+SO2↑+2H2O 由方程式可以看出2molH2SO4要1molCu ,Cu是足量的,但是随反应进行浓H2SO4的浓度会越来越稀,当反应到浓H2SO4变成稀H2SO4时这个反应就停止了,稀硫酸与铜不反应,含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数少于6.02×1023,故D错误;
CuSO4+SO2↑+2H2O 由方程式可以看出2molH2SO4要1molCu ,Cu是足量的,但是随反应进行浓H2SO4的浓度会越来越稀,当反应到浓H2SO4变成稀H2SO4时这个反应就停止了,稀硫酸与铜不反应,含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数少于6.02×1023,故D错误;
故选B。

【题目】实验室需要0.3 mol·L-1 NaOH溶液480 mL和一定浓度的盐酸溶液。根据这两种溶液的配制情况回答下列问题:

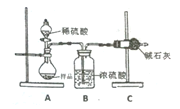
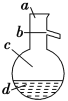
(1)如图所示的仪器中配制溶液肯定不需要的是_____________(填序号)。
(2)在配制NaOH溶液时:
填写下列表格:
应称取NaOH的质量/g | 应选用容量瓶的规格/mL |
__________________ | __________________ |
(3)容量瓶上需标有以下五项中的_________________(填序号)。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(4)下列配制的溶液浓度偏低的是________________________(填序号)。
A.配制前,容量瓶中有少量蒸馏水
B.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C.加蒸馏水时不慎超过了刻度线
D.定容时俯视刻度线
(5)下图为实验室某盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19g/mL
HCl的质量分数:36.5%
①该浓盐酸中HCl的物质的量浓度为_________molL-1。
②取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是____________
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
③在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有_________影响?(在横线上填“偏大”、“偏小”、“无影响”)。
Ⅰ溶液注入容量瓶前没有冷却至室温________
Ⅱ 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_________