题目内容
【题目】Ⅰ.汽车尾气排放的NOX和CO污染环境,在汽车尾气系统中安装催化转化器,可有效降低NOX和CO的排放。
已知:①2CO(g)+O2(g)![]() 2CO2(g), △H=-566.0kJ·mol-1
2CO2(g), △H=-566.0kJ·mol-1
②N2(g)+O2(g)![]() 2NO(g)△H=+180.5 kJ·mol-1
2NO(g)△H=+180.5 kJ·mol-1
回答下列问题:
(1)CO的燃烧热为___________,若1molN2(g)、1molO2(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1molNO(g)分子中化学键断裂时需吸收的能量为___________kJ。
(2)为了模拟反应2CO(g)+2NO(g)![]() 2CO2(g)+N2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
2CO2(g)+N2(g)在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用传感器测得不同时间NO和CO的浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4 kJ·mol-1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(10-3kJ·mol-1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前2s内的平均反应速率v(N2)___________。
②能说明上述反应达到平衡状态的是___________。
A.2n(CO2)=n(N2) B.混合气体的平均相对分子质量不变
C.气体密度不变 D.容器内气体压强不变
(3)在某恒容容器中发生下列反应:2NO2(g)![]() 2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率随温度变化如图所示。
2NO(g)+O2(g),将一定量的NO2放入恒容密闭容器中,测得其平衡转化率随温度变化如图所示。

该反应为___________反应(填“吸热”或“放热”),已知图中a点对应温度下,NO2的起始压强P0为120kPa,计算该温度下反应的平衡常数Kp的值为___________。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ.N2H4-O2燃料电池是一种高效低污染的新型电池,其装置如图所示:
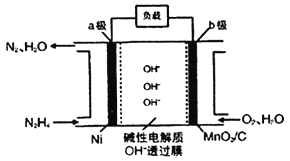
N2H4的电子式为___________;a极的电极反应方程式为___________;
【答案】 283kJ·mol-1 631.8 1.875×10-4mol/L·s) BD 吸热 81 ![]() N2H4-4e-+4OH-=N2+4H2O
N2H4-4e-+4OH-=N2+4H2O
【解析】Ⅰ(1)已知:①2CO(g)+O2(g)![]() 2CO2(g) △H=-566.0kJ·mol-1,则CO的燃烧热为566.0kJ
2CO2(g) △H=-566.0kJ·mol-1,则CO的燃烧热为566.0kJ ![]() =283kJ·mol-1;设1 mol NO(g) 分子中化学键断裂时需吸收的能量为x,由反应②可知,946 kJ+498 kJ-2x=+180.5 kJ,得x=631.8kJ,即1 mol NO(g) 分子中化学键断裂时需吸收的能量为631.75 kJ;(2)①根据化学反应速率之比等于计量数之比,由表中数据可知,前2s内的平均反应速率v(N2) =
=283kJ·mol-1;设1 mol NO(g) 分子中化学键断裂时需吸收的能量为x,由反应②可知,946 kJ+498 kJ-2x=+180.5 kJ,得x=631.8kJ,即1 mol NO(g) 分子中化学键断裂时需吸收的能量为631.75 kJ;(2)①根据化学反应速率之比等于计量数之比,由表中数据可知,前2s内的平均反应速率v(N2) =![]() v(NO)=
v(NO)=![]() ;②A、2n(CO2)=n(N2),反应开始时二氧化碳和氮气的量为0,根据化学计量,反应过程中生成的量始终为2n(CO2)=n(N2),无法判断是否达到平衡状态,选项A错误;B、该反应是气体体积缩小的反应,反应达到平衡状态前气体的物质的量始终不变,则气体的平均摩尔质量也发生变化,当容器内混合气体的平均相对分子质量保持不变时,说明达到了平衡状态,选项B正确;C、容器内混合气体的密度保持不变:该反应中气体的体积不变、质量不变,根据ρ=
;②A、2n(CO2)=n(N2),反应开始时二氧化碳和氮气的量为0,根据化学计量,反应过程中生成的量始终为2n(CO2)=n(N2),无法判断是否达到平衡状态,选项A错误;B、该反应是气体体积缩小的反应,反应达到平衡状态前气体的物质的量始终不变,则气体的平均摩尔质量也发生变化,当容器内混合气体的平均相对分子质量保持不变时,说明达到了平衡状态,选项B正确;C、容器内混合气体的密度保持不变:该反应中气体的体积不变、质量不变,根据ρ=![]() 可知,气体的密度始终不变,选项C错误;D、该反应是气体体积缩小的反应,反应达到平衡状态前气体的物质的量始终不变,则压强也发生变化,当容器内压强保持不变时,说明达到了平衡状态,选项D正确;答案选BD;(3)根据图中信息可知,温度升高平衡转化率增大,则升高温度平衡向正反应方向移动,正反应为吸热反应;
可知,气体的密度始终不变,选项C错误;D、该反应是气体体积缩小的反应,反应达到平衡状态前气体的物质的量始终不变,则压强也发生变化,当容器内压强保持不变时,说明达到了平衡状态,选项D正确;答案选BD;(3)根据图中信息可知,温度升高平衡转化率增大,则升高温度平衡向正反应方向移动,正反应为吸热反应;
2NO2(g)![]() 2NO(g)+O2(g)
2NO(g)+O2(g)
起始 P0 0 0
反应 0.6P0 0.6P0 0.3P0
平衡 0.4P0 0.6P0 0.3P0
K=![]() ;
;
Ⅱ.N2H4的电子式为![]() ;N2H4在a极失电子产生氮气,电极反应方程式为N2H4-4e-+4OH-=N2+4H2O。
;N2H4在a极失电子产生氮气,电极反应方程式为N2H4-4e-+4OH-=N2+4H2O。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案